Parkinsonin taudin historiaa
Tämä katsauksen tarkoituksena on kertoa saatavissa olevien kirjallisten lähteiden perusteella, miten Parkinsonin tautia tai sen tyypillisiä oireita, kuten vapinaa, on kuvattu ihmiskunnan historiassa ja miten sen hoito on kehittynyt varsinkin viimeisen 60 vuoden aikana. Toivottavasti katsauksesta on hyötyä sekä potilaille, heidän omaisilleen, potilasta hoitaville terveydenhuollon henkilöille ja tietysti myös muille taudista kiinnostuneille.
1. Ennen Kristuksen syntymää
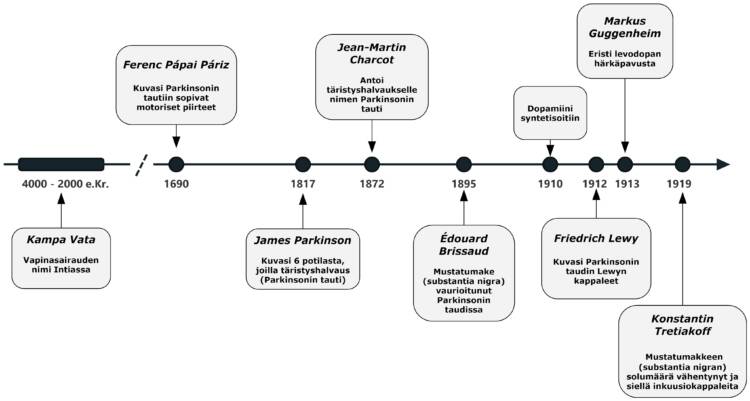
On mahdollista, että Parkinsonin tautia on ollut ihmiskunnassa sen koko olemassaolon ajan. Vanhimmat säilyneet kuvaukset Parkinsonin taudista ovat lähes 5000 vuotta ennen Kristuksen syntymää nykyisen Intian alueelta. Sanskritinkielisissä teksteissä Parkinsonin taudin nimenä on Kampa Vata (tai yhteen kirjoitettuna Kampavata). Näissä vanhoissa kuvauksissa on mahdollista, että osa potilaista on sairastanut Parkinsonin tautia tavallisempaa vapinasairautta eli essentiaalista vapinaa, mutta ainakin osalla on ollut todennäköisesti Parkinsonin tauti.
Mielenkiintoista on, että Kampa Vatan hoitoon käytettiin samettipavun siemeniä, joiden tiedetään sisältävän L-dopaa eli samaa lääkettä, joka on edelleenkin käytössä (nykyisin puhdistettuna L-dopana eli levodopana)[1, 2]. Sen ajan ihmiset eivät tietenkään tietäneet, mitä kemikaaleja siemenet sisälsivät, mutta kokemusperäisesti siis havaitsivat jo tuolloin levodopan suotuisan vaikutuksen oireisiin. Länsimaissa tämä asia keksittiin vasta 1960-luvun alussa, kuten myöhemmin ilmenee.
Myös muinaisessa Kiinassa tunnettiin Parkinsonin tauti paljon ennen Kristuksen syntymää. Nykyajan kemialliset analyysit ovat osoittaneet, että taudin hoitoon käytetyt perinteiset rohdostuotteet sisälsivät mm. antikolinergisiä ja monoamiinioksidaasi (MAO)-entsyymiä estäviä aineita, eli samoja lääkeaineita, joita nykyisinkin käytetään kemiallisesti valmistettuina Parkinsonin taudin hoitoon [3, 4]. Täten näillä rohdostuotteillakin on todennäköisesti ollut taudin oireita helpottavia vaikutuksia.
Raamatussakin on kuvauksia, jotka voisivat sopia Parkinsonin tautiin. Esim. Vanhassa testamentissa Saarnaajan kirjassa ”vartijat vapisevat ja voiman miehet käyvät koukkuisiksi” (Saarnaaja 12:3) ja Uudessa testamentissa Luukkaan evankeliumissa ”siellä oli nainen, jossa oli ollut heikkouden henki kahdeksantoista vuotta ja hän oli koukistunut ja täydelleen kykenemätön oikaisemaan itsensä” (Luukas 13:11).
2. Antiikin aika
Antiikin ajalta ehkä selkein kuvaus Parkinsonin taudin oireista on kreikkalaisen lääkärin Galenin (129-200) kirjoitukset erilaista vapinoista. Hän erotti lepovapinan (tyypillinen Parkinsonin taudille) liikkeen aikana tapahtuvasta vapinasta (tyypillinen essentiaaliselle vapinalle)[5]. Galen oli hyvin monipuolinen lääkäri, jonka monet anatomiset ja farmakologiset opit olivat käytössä uudelle ajalle saakka.
3. Keskiaika
Mona Lisa -maalauksestaan tunnettu italialainen taiteilija Leonardo Da Vinci (1452-1519) maalaustaiteen ohella hyvin monipuolinen henkilö, lähinnä voisi sanoa keksijä. Lääketieteen alalla hän oli erityisesti anatomisti. Säilyneissä kirjoituksissaan hän on kuvannut myös vapisevia henkilöitä, joilla todennäköisesti oli Parkinsonin tauti [6]. Onpa jopa epäilty, että hän itsekin olisi sairastanut Parkinsonin tautia.
4. Uusi aika – 1950
Jo 1690 unkarilainen lääkäri Ferenc Pápai Páriz kuvasi todennäköisesti ensimmäisenä Parkinsonin taudin kaikki motoriset pääpiirteet eli vapinan (tremor), hitauden (bradykinesia), jäykkyyden (rigiditeetti) ja asennon muutokset [7]. Hän kirjoitti unkariksi ja tämän vuoksi hänen kirjoituksensa ei levinnyt kovin laajaan tietoisuuteen. 1700-luvulta on myös useita artikkeleita. joissa kuvataan todennäköisesti Parkinsonin tautia sairastavia potilaita [8].
Varsinainen Parkinsonin taudin raportointi tapahtui vuonna 1817, kun englantilainen apteekkari-kemisti James Parkinson (1755-1824) kuvasi kuusi miespotilasta kirjassaan ”An Essay on the Shaking Palsy” (”Tutkielma täristyshalvauksesta”)[9, 10]. Tämän tutkielman perusteella hän on jäänyt historiaan Parkinsonin taudin nimessä, vaikka hän siis ei itse tätä nimeä käyttänytkään. Itse hän tutki kolme potilasta ja kolme muuta hän näki kävelevän kadulla. James Parkinson kuvaili taudille luonteenomaisen vapinan ja hitauden sekä kävelyn ja asennon muutokset. Hän raportoi potilailla olevan myös unihäiriöitä, puhevaikeuksia, nielemisen ongelmia, syljen valumista, rakon toiminnan häiriöitä ja ummetusta. Sen sijaan hän ei havainnut jäykkyyttä eli rigiditeettiä. James Parkinsonilla ei ehdottanut mitään erityistä nykypäivänä ajatellen tehokasta hoitoa tautiin. Hän suositti mm. elohopean käyttöä, kuppausta ja märkivän rakkulan tekoa niskan iholle. Hän suositti myös monipuolista ravintoa, joka ohje on edelleenkin pätevä.
Vasta runsaat 50 vuotta myöhemmin kuuluisa ranskalainen neurologi Jean-Martin Charcot (1825-1893) alkoi käyttää termiä Parkinsonin tauti [11]. Erityisesti hän halusi poistaa sanan halvaus (palsy), koska Parkinsonin taudissa potilailla ei ole varsinaista halvausta, kuten esim. aivoinfarktipotilailla. Charcot havaitsi myös Parkinson-potilaiden jäykkyyden. Hän havaitsi myös, että hyoskyamiini voi helpottaa potilaiden oireita. Hyoskyamiini on eräs belladonna-alkaloidi (”bella donna” = kaunis nainen; aineesta tehdyt silmätipat aiheuttavat laajat silmäterät) ja se sisältää skopolamiinia, antikolinergistä ainetta, jonka tiedetään helpottavan erityisesti vapinaa (antikolinergi tarkoittaa ainetta, joka estää hermovälittäjäaineen asetyylikoliinin vaikutusta). Luonnon antikolinergiset aineet, erityisesti atropiini ja sen johdokset, olivatkin länsimaissa tärkein Parkinsonin taudin lääkehoito aina 1950-luvulle saakka.
Vuonna 1910 syntetisoitiin dopamiini lääketehdas Wellcomen laboratoriossa Lontoossa [12], mutta vasta runsaat 40 vuotta myöhemmin tiedettiin, että dopamiinia on aivoissa ja että se on tärkeä hermovälittäjäaine.
Ranskalainen patologi Édouard Brissaud (1852-1909) lienee ensimmäinen, joka arveli mustatumakkeen (substantia nigran) olevan vaurioituneen Parkinsonin taudissa vuonna 1895 [10]. Varsinaisesti tämän osoitti venäläinen neuropatologi Konstantin Tretiakoff (1892-1956) vuonna 1919 väitöskirjassaan ollessaan 27-vuotias [13]. Hän havaitsi, että Parkinsonin tautia sairastavilla potilailla pigmentoituneiden solujen määrä oli vähentynyt substantia nigrassa. Hän havaitsi myös, että substantia nigran soluissa oli ylimääräisiä kertymiä eli inkluusiokappaleita. Nämä kappaleet oli saksalainen (sittemmin amerikkalainen) Friedrich Lewy (1885-1950) havainnut jo muutama vuosi aiemmin (v. 1912) tutkiessaan Parkinsonin taudin potilaiden aivoja [14]. Substantia nigran Lewyn kappaleet ovat edelleen eräs tärkeimmistä neuropatologista löydöksistä Parkinsonin taudissa.
Suomenkielisessä lääketieteellisessä aikakauskirja Duodecimissa (alkoi ilmestyä v. 1885) on ensimmäinen kuvaus Parkinsonin taudista vuodelta 1890 [15]. Kyseessä on piirilääkäri Konrad Relanderin suomennos kuuluisan saksalaisen neurologin prof. Wilhelm Heinrich Erbin (1840-1921) edellisenä vuonna pitämästä esitelmästään erilaisista hermotaudeista. Parkinsonin taudin mainitaan olevan ”sellainen tauti, jossa diagnosi tavallisesti on helppo”. Vapinasta käytetään sanaa ”väräjäminen”, ”joka usein ajoittain, jopa tykkönäänkin voi puuttua”.
Vuosina 1917-1926 maailmassa riehui aivokuume (unitauti, encephalitis lethargica, von Economon tauti), jonka seurauksena monet sairastuivat Parkinsonin taudin kaltaiseen tautiin, josta käytettiin nimeä post-enkefaliittinen parkinsonismi [16]. Aivokuumeen varma syy on jäänyt avoimeksi, mutta mm. influenssavirusta on epäilty taudin aiheuttajaksi. Amerikkalainen neurologi Oliver Sacks kirjoitti tästä taudista kirjan nimeltä Heräämisiä (Awakenings), joka ilmestyi vuonna 1973. Vuonna 1990 kirjasta ilmestyi myös samanniminen elokuva, jossa Robert De Niro esittää parkinsonismipotilasta, joka ”herää henkiin” saatuaan levodopalääkitystä, mutta varsin nopeasti hänelle valitettavasti kehittyivät myös tyypilliset pakkoliikkeet eli dyskinesiat. Näit potilaita ei liene enää elossa.
5. 1950-luku
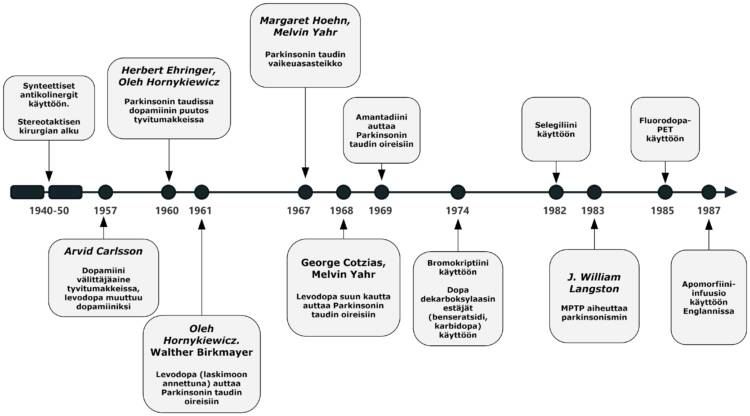
1940-luvun lopulla kehitettiin stereotaktinen laitteisto, jonka avulla pystyttiin osumaan tarkasti pieneenkin kohteeseen aivoissa. Eräs kuuluisimmista laitteen kehittäjistä oli ruotsalainen neurokirurgi Lars Leksell (1907-1986) [17]. Stereotaktisten tekniikan avulla suoritettiin 1950- ja 60-luvuilla Parkinsonin tautia sairastaville potilaille paljon leikkauksia, joissa tehtiin pysyvä vaurio talamus-tumakkeeseen (talamotomia) tai pallidum-tumakkeeseen (pallidotomia). Nämä leikkaukset tehtiin pääsääntöisesti toispuoleisesti ja ne auttoivat erityisesti vastapuolen vapinaan ja jäykkyyteen. Molemminpuolisiin leikkauksiin liittyi selvästi suurentunut haittavaikutusten riski, kuten puheen huonontuminen, näköhäiriöt ja ajatustoiminnan häiriöt. Suomalainen neurokirurgi Lauri V. Laitinen (1929-2005) suoritti Töölön sairaalassa Helsingissä runsaasti näitä leikkauksia erityisesti 60-luvulla. Myöhemmin hän jatkoi uraansa Bergenissä, Uumajassa ja Tukholmassa [18]. Hän oli erittäin arvostettu maailmanlaajuisesti Parkinsonin taudin potilaiden neurokirurgisesta hoidosta. Hän myös kehitti edelleen Leksellin stereotaktista laitteistoa.
1950-luvulla lääkkeistä tärkeimpiä olivat synteettiset antikolinergiset aineet, kuten triheksifenidyyli eli bentsheksoli (Artane), bents(a)tropiini (Cogentin), biperideeni (Akineton; joka on edelleen markkinoilla), orfena(n)driini (Disipal, Norflex) ja prosyklidiini (Kemadrin) [19]. Osa aineista oli enemmän antihistamiineja, kuten difenhydramiini (Benadryl) tai prometatsiini (Phenergan) [20]. Näillä oli kohtalaisesti tehoa erityisesti vapinaan, mutta myös huomattavasti haittoja, esim. suun kuivumista, ummetusta, rakon toiminnan häiriöitä ja erityisesti keskushermoston haittoja, kuten muistin huonontumista, väsymystä ja harhoja. Mainittakoon, että myös apomorfiinin suotuisa mutta lyhyt vaikutus Parkinsonin oireisiin havaittiin jo 1950-luvun alussa [21]. Sen vaikutusmekanismia (=dopamiiniagonisti, ks myöhemmin) ei silloin tiedetty. Se jäikin lähes unholaan aina 1980 luvun lopulle saakka (ks. myöhemmin), koska sen teho suun kautta otettuna oli huono ja se aiheutti pahoinvointia ja oksentelua ja mahdollisesti munuaisvaurioitakin.
1950-luvun loppupuolella tapahtui sitten suuri mullistus Parkinsonin taudin historiassa. Ensin ruotsalainen farmakologi Arvid Carlsson (1923-2018) havaitsi, että erityisesti tyvitumakkeiden alueella on paljon dopamiinia ja että se on itsenäinen välittäjäaine eikä pelkästään esiaste toiselle tunnetulle välittäjäaineelle, noradrenaliinille, kuten siihen saakka oli luultu. Lisäksi hän osoitti, että reserpiini (vanha verenpainelääke) aiheuttaa kaneilla parkinsonismin kaltaisen tilan, joka oli estettävissä levodopalla, joka muuttuu aivoissa dopamiiniksi. Nämä havainnot hän julkaisi kahtena yhden sivun mittaisena artikkelina vuosina 1957 ja 1958 arvostetuissa tiedelehdissä Nature [22] ja Science [23]. Luonnollisesti hän on julkaissut runsaasti pidempiäkin artikkeleita erityisesti dopamiiniin liittyen [24]. Näistä saavutuksistaan hänelle myönnettiin Nobelin palkinto vuonna 2000 (yhdessä amerikkalaisten hermotutkijoiden Paul Greengardin ja Eric Kandelin kanssa).
6. 1960-luku
Hyvin pian Arvid Carlssonin eläintutkimisten jälkeen osoitettiin, että Parkinsonin tautia sairastaneiden potilaiden aivojen (erityisesti tyvitumakkeiden) dopamiinipitoisuus oli huomattavasti alentunut. Suurin kunnia tästä menee itävaltalaiselle farmakologille Oleh Hornykiewiczille (1926-2020), joka vuonna 1960 julkaisi löydöksen yhdessä Herbert Ehringerin (1932-2023, sittemmin sisätautilääkäri) kanssa paikallisessa saksankielisessä tiedelehdessä [25]. Vuosi myöhemmin (1961) Oleh Hornykiewicz yhdessä neurologi Walther Birkmayerin (1910-1996) kanssa osoitti, että laskimoon annettuna levodopa poisti pitkään sairastaneiden Parkinson-potilaiden oireet lyhyeksi ajaksi [26]. Potilaat tavallaan heräsivät henkiin, nousivat vuoteesta ja lähtivät kävelemään. Oli keksitty ensimmäinen todella tehokas lääkehoito Parkinsonin tautiin. Hornykiewiczin kanssa samanaikaisesti japanilainen Isamu Sano (1924-1975) raportoi myös dopamiinin puutoksen ja laskimoon annetun D,L-dopan lyhyen suotuisan vaikutuksen Parkinsonin taudissa [27]. Hänen alkuperäisjulkaisu oli japaniksi ja sai siten vähän huomiota länsimaissa. Näiden havaintojen jälkeen alkoi dopamiinin korvaushoidon aikakausi Parkinsonin taudissa, jota edelleenkin elämme [28-30]. Mainittakoon, että aineena D,L-dopa on tunnettu jo yli sata vuotta, sillä puolalais-amerikkalainen biokemisti Casimir (Kazimierz) Funk (1884-1967) syntetisoi sen vuonna 1911 [31] ja lääketehdas Hoffman-La Rochen kemisti Marcus Guggenheim (1884-1967) eristi levodopan (L-dopan) härkäpavusta vuonna 1913 [32]. Hän myös kokeili levodopan vaikutusta nauttimalla sitä suun kautta 2,5 g ja huomasi sen aiheuttavan pahoinvointia ja oksentelua.
Kuitenkin koko 1960-luvun ajan kiisteltiin siitä, onko levodopa tehokas Parkinsonin taudissa. Esimerkiksi prof. Urpo Rinne (1935-) ja dos. Vesa Sonninen (1935-2015) raportoivat Turusta v. 1968, että laskimoon annetulla levodopalla annoksella 1,5 mg/kg ei saatu merkittävää välitöntä vaikutusta Parkinsonin taudin oireisiin, kun verrattiin lumelääkkeenä käytettyyn keittosuolaliuokseen [33]. Ainoastaan 6 tunnin kohdalla liikkumiskyky oli hieman parempi levodopaa saaneilla potilailla. Eräs syy ristiriitaisiin tuloksiin oli, että puhdasta levodopaa oli vaikea saada ja sen sijaan käytettiin D,L-dopaa, jossa D-dopa on tehoton komponentti. Toisena syynä huonoihin tuloksiin oli, että suun kautta annetut D,L-dopan tai levodopan annokset olivat liian pieniä. Vasta 1960-luvun lopulla amerikkalaiset neurologit (alun perin kreikkalainen) George Constantin Cotzias (1918-1977) ja Melvin Yahr (1917-2004) osoittivat selvästi, että D,L-dopa ja myöhemmin levodopa auttavat Parkinsonin taudin oireisiin, kunhan suun kautta annettava levodopan annos on yli 5-6 grammaa päivässä [34-36]. Näin suurten annosten käyttö vaati hitaan annoksen noston mm. pahoinvoinnin ja oksentelun estämiseksi. Havaittiin myös, että jo vuoden sisällä valtaosalle potilaista alkoi kehittyä tahattomia liikkeitä eli dyskinesioita. Hyvin pian Cotziaksen tulosten jälkeen (v. 1969) prof. Erkki Kivalo (1920-2009) työtovereineen Helsingistä julkaisi ensimmäiset positiiviset tulokset levodopalla suomalaisilla potilailla keskimääräisen annoksen ollessa 4 g/vrk suun kautta [37]. Vähän myöhemmin (v. 1971) myös prof. Urpo Rinne työtovereineen Turusta raportoi suun kautta annetun levodopan merkittävästi vähentävän Parkinson-potilaiden oireita [38]. Heidän tutkimuksissaan levodopan annos vaihteli 1,5 g -7,5 g/vrk.
Levodopan ohella amantadiinin Parkinsonin tautia lievittävä vaikutus keksittiin sattumalta 1960-luvun lopulla. Amantadiini (Atarin) oli kehitetty influenssan estolääkkeeksi ja annettaessa sitä tällä perusteella Parkinson-potilaille he havaitsivat sen hyödyllisen vaikutuksen oireisiinsa [39]. Amantadiini on varsin heikkotehoinen ja sen käyttö oli vähäistä aina 2000-luvulle saakka. Tällöin havaittiin sillä olevan tahattomia liikkeitä eli dyskinesioita vähentävää vaikutusta ja tämä havainto on uudelleen lisännyt sen käyttöä. Vuosina 2017 ja 2018 USA:ssa hyväksyttiin käyttöön pitkävaikutteiset amantadiinivalmisteet Gocovri; Osmolex), joita voidaan annostella vain kerran päivässä, kun tavanomaista amantadiinia käytetään yleensä kolme kertaa päivässä.
Vuonna 1967 amerikkalaiset neurologit Margaret Hoehn (1930-2005) ja Melvin Yahr (1917-2004) julkaisivat Parkinsonin taudin viisi-portaisen Parkinsonin taudin vaikeusasteikon, joka on edelleen käytössä hieman täydennettynä ja kulkee Hoehn et Yahr asteikon nimellä [40].
7. 1970-luku
Ratkaiseva parannus levodopa-hoidossa saatiin 1970-luvun alkupuolella, kun keksittiin levodopaa hajottavan entsyymin, dopa dekarboksylaasin eli aromaattisten aminohappojen dekarboksylaasin, estäjät, karbidopa ja benseratsidi [41]. Niiden avulla levodopan annos voitiin pienentää noin kymmenesosaan. Samalla myös monet levodopan haittavaikutukset vähenivät huomattavasti. Lääketehtaat alkoivatkin myydä valmisteita, joissa levodopa ja karbidopa (Sinemet) tai levodopa ja benseratsidi (Madopar) ovat samassa tabletissa. Nämä levodopa-valmisteet tulivat markkinoille vuosien 1973-74 aikana ja ovat edelleen runsaasti käytössä.
1970-luvulla keksittiin, että dopamiinilla on aivoissa useampia erilaisia vaikutuskohtia eli reseptoreita [42]. Lääketehtaat alkoivat kehittää lääkeaineita, jotka vaikuttivat suoraan näihin reseptoreihin toisin kuin levodopa, joka muuttuu aivoissa ensin dopamiiniksi. Eräs ensimmäisistä tällaisista suoraan dopamiinireseptoreihin vaikuttavista aineista eli dopamiiniagonisteista, joilla on Parkinson taudin oireita vähentävää vaikutusta, oli bromokriptiini (Parlodel)[43, 44]. Se tuli markkinoille vuonna 1974 ja on edelleenkin saatavilla, mutta ei enää ensisijainen agonisti. Se eristettiin torajyvästä, jonka vuoksi sitä ja sen myöhempiä johdoksia (kuten pergolidi (Permax), markkinoille 1982 ja kabergoliini (Cabaser), markkinoille 1990) kutsutaan torajyväalkaloideiksi eli ergot-alkaloideiksi. Varsin pian havaittiin, että ergot-johdoksiin liittyi haittavaikutuksena keuhkopussin tulehduksen kaltainen tila tai pahimmassa tapauksessa sidekudoksen kertyminen keuhkoihin eli keuhkofibroosi. Myöhemmin 2000-luvulla havaittiin vielä, että ergot-johdokset voivat aiheuttaa sydämen läppävikoja. Näiden haittojen vuoksi ergot-lääkkeiden käyttö on huomattavasti vähentynyt ja esim. pergolidin myynti lopetettiin vuonna 2007.
Ergot-johdosten tilalle kehitettiin 1980-luvulla rakenteellisesti muunlaisia dopamiiniagonisteja, joista runsaassa käytössä ovat edelleen ropiniroli (Requip, markkinoille 1996, Suomessa 2003) ja pramipeksoli (Sifrol, markkinoille 1997). Myöhemmin on tullut lisäksi laastarimuotoinen agonisti rotigotiini (Neupro, markkinoille 2005)[45]. Myös aiemmin mainittu apomorfiini kuuluu tähän ryhmään.
8. 1980-luku
Vuonna 1979 kuvattiin 23-vuotiaan opiskelijapojan sairastuneen muutaman viikon sisällä Parkinsonin taudin kaltaiseen tautiin, kun hän oli käyttänyt itse syntetisoimaa petidiinin kaltaista huumetta [46]. Tällöin ei vielä tiedetty syytä asiaan, mutta 1980-luvun alussa samanlaisia tapauksia ilmeni useita Kaliforniassa. Neurologi J. William Langston selvitti, että kyseinen myrkyllinen aine oli MPTP (metyylifenyylitetrahydropyriidiini)[47]. Tämä havainto johti ensinnäkin Parkinsonin taudin eläinmallin kehittämiseen (erityisesti apina ja hiiri) ja toiseksi alettiin etsiä luonnosta tai ravinnosta mahdollisia muita vastaavia kemikaaleja, jotka voisivat olla Parkinsonin taudin syynä. Toistaiseksi varmuudella tällaista kemikaalia tai kemikaaleja ei ole kuitenkaan löydetty.
Dopamiiniagonistien ohella jo 1970-luvulla aloitettiin monoamiinioksidaasin tyyppi B:tä estävien lääkkeiden eli MAO B-estäjien kehitystyö. MAO B on entsyymi, joka hajottaa aivoissa dopamiinia ja siten sen estämisellä pystytään nostamaan tai ”säästämään” aivojen dopamiinia. Ensimmäinen tehokas MAO B-estäjä oli l-deprenyyli eli selegiliini (Eldepryl), joka on unkarilaisen farmakologin Joseph Knollin (1925-2018) tutkimustyön tulosta [48]. Selegiliini tuli markkinoille v. 1982, Suomen ollessa eräs ensimmäisiä maita sen käyttäjänä. Selegiliinille on vuosien kuluessa kehitetty useampiakin kilpailijoita, mutta mikään niistä ei ole ollut sitä parempi eivätkä ne ole tulleet varsinaiseen kliiniseen käyttöön. Vasta israelilaisen tutkimusryhmän kehittämä MAO B-estäjä rasagiliini on tullut selegiliinin kilpailijaksi vuonna 2005 [49]. Kolmas käytössä oleva MAO B-estäjä on safinamidi (Xadago), joka tuli markkinoille Euroopassa 2015 [50]. Se on toistaiseksi hyväksytty käytettäväksi vain lisälääkkeenä levodopan ja muiden Parkinson-lääkkeiden kanssa.
Kun saatavilla oli useammalla eri tavalla dopamiiniin vaikuttavia lääkkeitä, oli luonnollista, että niitä ruvettiin käyttämään myös yhdessä. Yhdistelmissä kunkin lääkkeen annostus voidaan pitää pienempänä ja siten myös niiden haitat saattavat olla vähäisempiä, mutta teho saattaa silti olla parempi. Tällainen dopaminergisten lääkkeiden yhdistelmäkäyttö, esim. levodopan, dopamiiniagonistin ja MAO B-estäjän yhdistelmä, on edelleenkin paljon käytössä. Kun lisäksi jo varhain havaittiin, että levodopan pitkäaikaiskäyttöön liittyy ongelmia, kuten vaikutusajan lyhentymistä ja tahattomia liikkeitä, alettiin suosia lääkityksessä erityisesti alkuvaiheessa ja nuoremmilla potilailla, dopamiiniagonistien ja MAO B-estäjien käyttöä [51].
1980-luvun puolivälissä pystyttiin ensimmäisen kerran havainnollistamaan elävän ihmisen aivojen dopamiinia käyttämällä fluorodopaa ja PET-kuvausta (positroniemissiotomografia)[52]. Pian tämän jälkeen osoitettiin, että Parkinsonin taudissa kertymä on alentunut ja siten menetelmää voidaan käyttää Parkinsonin taudin diagnoosin tueksi [53]. Tätä PET-menetelmää käytetään edelleen paljon erityisesti tutkimustyössä, esimerkiksi eräänä menetelmänä aineiden neuroprotektiota arvioitaessa. Potilastyössä käytetään enemmän halvempaa menetelmää, dopamiinitransportteri-SPECT- (tai SPET eli yksifotoniemissiotomografia)(DaT-Scan) tutkimusta, joka sekin on ollut käytettävissä 1990-luvulta lähtien [54, 55]. Dopamiinitransportteri-SPECT on nykyisin käytettävissä Suomen kaikissa keskussairaaloissa.
9. 1990-luku
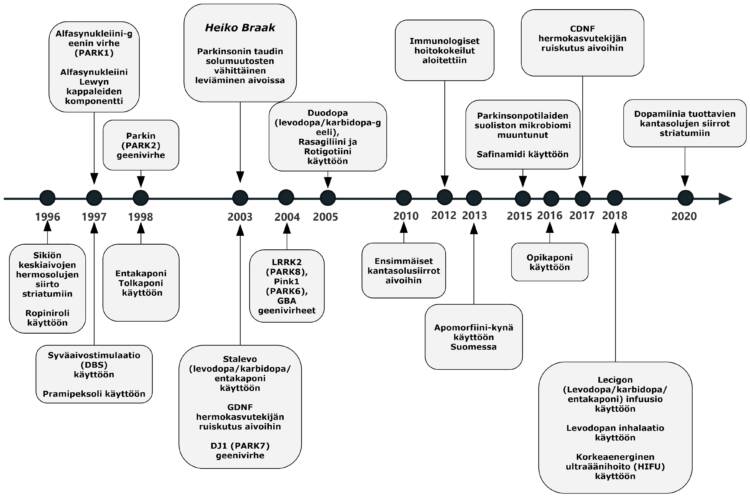
1990-luvulla tulivat käyttöön katekoli-O-metyylitransferaasin estäjät eli COMT-estäjät [56]. COMT on entsyymi, joka hajottaa levodopaa jo suolessa, maksassa ja verenkierrossa, niin ettei aivoihin mene kuin pieni osa levodopasta. COMT:n merkitys korostuu, kun levodopatableteissa on mukana jo toinen entsyymin estäjä eli dopadekarboksylaasin estäjä (benseratsidi tai karbidopa, ks. edellä). COMT-estäjä liitetään siis aina levodopaan sen vaikutusta parantamaan ja pidentämään eikä sillä itsellään ole vaikutusta Parkinsonin oireisiin [57]. Entakaponi (Comtess, Comtan) on eniten käytetty COMT-estäjä. Se tuli markkinoille v. 1998. Entakaponin kehitystyö on tehty Suomessa suomalaisten farmakologien, neurologien ja lääketehdas Orionin yhteistyönä [58, 59]. Tämän kehitystyön ”isä” on Helsingin yliopiston farmasian laitoksen farmakologian emeritusprofessori Pekka Männistö. Suomalaisten ohella samanaikaisesti sveitsiläinen lääketehdas Hoffman-La Roche kehitti oman COMT-estäjän, tolkaponin (Tasmar), joka tuli muutamaa kk:ta aiemmin markkinoille kuin entakaponi [60]. Tolkaponin ”isänä” voidaan pitää professori Mose Da Pradaa (1934-1995), joka teki pitkän päivätyön Rochen palveluksessa. Tolkaponin käyttöön on liittynyt maksavaurion vaara, jonka vuoksi sen käyttö on jäänyt selvästi entakaponia pienemmäksi. Vuonna 2016 markkinoille tuli kolmas COMT-estäjä, opikaponi (Ongentys). Nykyisin entakaponi on yhdistetty samaan tablettiin yhdessä levodopan ja karbidopan kanssa (Stalevo, markkinoille v. 2003). Potilaan kannalta tämä on miellyttävämpää, kun ei tarvitse käyttää kuin yhtä tablettia kerrallaan.
1990-luku toi mukanaan myös neurokirurgian uuden tulemisen Parkinsonin taudin hoidossa. Vuonna 1992 Lauri V. Laitinen (tällöin Tukholmassa) julkaisi, että pallidotomia hyödyttää tilanvaihteluista kärsiviä Parkinson-potilaita [61]. Tämäntapaiset vaurioleikkaukset kuitenkin jäivät nopeasti historiaan, kun keksittiin, että johtamalla jatkuvasti sähkövirtaa korkealla taajuudella aivoihin elektrodin kautta voidaan saada aikaan sama tai parempi vaste kuin tekemällä pysyvä vaurio. Näin alkoi aivojen stimulaatiohoito (deep brain stimulation eli DBS), jota kehitti erityisesti ranskalainen neurokirurgi Alim-Louis Benabid (1942-)[62]. DBS:n etuna on, että se aiheuttaa hyvin pienen vaurion aivoihin ja sen voidaan asentaa molemminpuolisesti. Tutkimuksissa havaittiin, että paras hyöty saadaan asentamalla stimulaatioelektoridit subtalaamiseen tumakkeeseen, mutta hyötyä saatiin myös palldumiin tai talamukseen (erityisesti vapinan ollessa ongelma) asennetuista elektrodeista. DBS-hoito auttaa erityisesti potilaita, jolla on levodopa-hoitoon liittyviä voimakkaita päivittäisiä tilanvaihteluja ja tahattomia liikkeitä, tai potilaita, joilla on vaikea vapina [63]. 2010-luvun lopulla otettiin käyttöön suuntaavat elektrodit, joilla voidaan kohdistaa stimulaatio tarkemmin ja vähentää DBS:n aiheuttamia haittoja [64].
1990-luvulla tehtiin myös ensimmäiset hermosolujen siirrot Parkinson-potilaiden aivoihin. Tämä hoitomuodon kehitys alkoi itse asiassa siitä, että meksikolaiset lääkärit v. 1987 raportoivat lisämunuaisen ytimen solujen siirtämisen Parkinson-potilaiden aivoihin vähentävän potilaiden oireita [65]. Lisämunaisen ytimessä on ns. katekoliamiinisoluja, jotka voivat tuottaa dopamiinia, noradrenallinia ja adrenaliinia. Varsin pian kuitenkin osoitettiin, että lisämunuaisen solut eivät elä aivoissa eivätkä tuota dopamiinia. Tämän vuoksi siirryttiin käyttämään abortoidun sikiön keskiaivojen soluja, jotka pystyvät erilaistumaan dopamiinisoluiksi ja ovat itse asiassa verrattavissa pitkälle kantasoluihin [66, 67]. Näitä siirrettiin Parkinson-potilaiden tyvitumakkeisiin useissa keskuksissa maailmassa 90-luvulla, mm. Lundissa Ruotsissa, mutta ei Suomessa. Tutkimuksissa osoitettiin, että siirretyt solut pysyvät hengissä ja erilaistuvat dopamiinisoluiksi ja vähentävät potilaiden oireita. Nämäkin hoidot kuitenkin käytännössä lopetettiin 2000-luvun alkupuolella, kun tieteellisesti hyvin tehdyt tutkimukset osoittivat, että vain osa potilaista sai hyötyä ja yli puolelle kehittyi haittavaikutuksia, erityisesti pahoja tahattomia liikkeitä [68, 69].
1990-luvun loppupuolella selvisi ensimmäinen Parkinsonin taudin geenivirhe, joka havaittiin alfa-synukleiinin geenissä (SNCA) italialais-kreikkalaisissa suvuissa v. 1997 [70]. Tämän geenivirheen sairaudelle annettiin nimeksi PARK1. Samanaikaisesti havaittiin, että valkuaisaine alfa-synukleiini on tärkein Lewyn kappaleiden komponentti [71]. Nämä havainnot johtivat sekä useiden uusien geenivirheiden löytymiseen Parkinsonin taudissa että alfa-synukleiinin merkityksen tutkimiseen hermosolukuolemassa erityisesti 2000-2010-lukujen puolella. Yhden geenin virheen aiheuttamia Parkinsonin tauteja tai parkinsonismeja tunnetaan nykyisin noin 20 ja lisäksi tunnetaan lukuisia muita geenipaikkoja, jotka kytkeytyvät Parkinsonin tautiin [72]. Tavallisin vallitsevasti periytyvä muoto on LRKK2 geenin mutaatioista johtuva tauti (PARK8) ja tavallisin peittyvästi periytyvä muoto on parkin geenin (PRKN) mutaatioista johtuva tauti (PARK2). Kuitenkin geneettiset virheet selittävät vain noin 5-10 % Parkinsonin taudin syistä. Valtaosa Parkinsonin taudin tapauksista ajatellaan siis johtuvan ns. ulkoisista syistä, joita edelleen kiivaasti etsitään. Geneettisten syiden löytymisestä on ollut paljon hyötyä perustutkimukselle, kun niiden avulla on selvinnyt erilaisia solukuoleman mekanismeja, kuten esimerkiksi mitokondrioiden tärkeä rooli tässä tapahtumassa [73]. Ne ovat myös avanneet erilaisia mahdollisuuksia pyrkiä estämään Parkinsonin taudin etenemistä ja monia ns. neuroprotektiivisia hoitokokeiluja on 2000-luvun alusta lähtien tapahtunut, mutta valitettavasti tehokasta yhdistettä ei ole vielä löytynyt [74].
10. 2000-luku
2000-luvun alussa saksalainen anatomisti Heiko Braak (1937-) esitti, että Parkinsonin taudin solumuutokset alkavat aivorungon tumakkeista ja nousevat sieltä vaiheittain ylöspäin aina aivokuorelle saakka [75]. Osalla leviäminen tapahtuu myös hajutumakkeen kautta. Jokin patogeeni (kuten virus tai bakteeri) voisi nousta suolistosta hermoja pitkin aivorunkoon tai hajuhermojen kautta kulkeutua aivoon. Tämä ns. Braakin hypoteesi on saanut paljon huomiota. Monen potilaan kohdalla se näyttäisi pitävän paikkansa, mutta on myös Parkinsonin tautia sairastavia potilaita, joihin se ei sovi [76].
2000-luvulla alettiin kiinnittämään yhä enemmän huomiota parkinsonpotilaiden ei-motorisiin oireisiin, kuten hajuaistin huonontumiseen, ummetukseen, virtsarakon toiminnan häiriöihin, impotenssiin, psyykkisiin oireisiin, muistihäiriöihin, unihäiriöihin ja kipuihin [77]. Havaittiin, että osa oireista, kuten hajuaistin huonontuminen, ummetus, masennus ja REM-unen aikainen häiriö (RBD) voivat edeltää vuosia ennen motorisia oireita. Havaittiin myös, että Parkinsonin taudin dopaminergiset lääkkeet, erityisesti dopamiiniagonistit, voivat lisätä impulssikontrollihäiriöitä, kuten ostoshimoa, pelihimoa, hyperseksuaalisuutta ja ruuan ahmimista [78]. Prof. Juho Joutsan ryhmä Turusta on tutkinut ansiokkaasti suomalaisten parkinsonpotilaiden impulssikontrollihäiriöitä [79].
2000-luku toi mukanaan vielä levodopan erään uuden tulemisen, nimittäin sen jatkuvan infuusion ohutsuoleen kannettavan pumpun avulla mahaan tehdyn avanteen kautta (PEG). Tämän geelimäisen levodopan (Duodopa, markkinoille v. 2005) avulla saavutetaan varsin tasaiset veripitoisuudet ja sillä tavoin pitkään sairastaneiden potilaiden tilanvaihteluja ja tahattomia liikkeitä voidaan vähentää [80]. Tämä hoito on pääosin kehitetty Uppsalassa prof. Sten-Magnus Aquiloniuksen (1939-) ja dos. Dag Nyholmin (1974-) johdolla. Hoito on varsin kallista ja teknisesti myös aika vaativaa ja siten soveltuu vain tarkoin harkituille potilaille [81]. Sama ryhmä kehitti hoitoa eteenpäin lisäämällä entakaponin levodopa/karbidopa-infuusioon (Lecigon)[82]. Se tuli markkinoille Ruotsissa v. 2018 ja Suomessa 2019. Entakaponin ansiosta levodopan määrää voidaan pienentää ja tämä osaltaan mahdollistaa pienemmän pumpun käytön.
2000-luvun alkupuolella aloitettiin hermon kasvutekijöiden vaikutusten tutkiminen Parkinsonin taudissa. Hermon kasvutekijät ovat valkuaisaineita, joita tarvitaan hermoston kehityksessä, mutta myös myöhemmin hermosolujen elossa pidossa. Eläintutkimuksissa havaittiin, että GDNF-niminen kasvutekijä on tärkeä dopamiini-solujen elossa pidossa. Sitä ruiskutettiin pumpun avulla parkinson-potilaiden tyvitumakkeisiin ja alustavat tutkimukset osoittivat, että siitä on hyötyä [83]. Kuitenkin kontrolloiduissa tutkimuksissa tulokset olivat kyseenalaiset ja tutkimukset tämän aineen kohdalta lopetettiin [84]. Tämä tutkimuslinja on jatkumassa, koska uusia hermon kasvutekijöitä on keksitty, joilla voisi olla vaikutusta Parkinsonin taudin kulkuun. Eräs tällainen tekijä on Helsingin yliopiston prof. Mart Saarman löytämä CDNF-niminen kasvutekijä. Sillä tehtiin alustava tutkimus suomalaisilla ja ruotsalaisilla parkinsonpotilailla, jossa se todettiin turvalliseksi aivoon ruiskutettuna, mutta kliininen vaste jäi epävarmaksi, johtuen osin pienestä potilasmäärästä [85].
11. 2010-luku
2010-luvun alussa raportoitiin ensimmäiset Parkinson-potilaille tehdyt kantasolusiirrot. Kyseessä oli potilaiden omasta luuytimestä eristettyjen kantasolujen siirto toispuoleisesti striatumiin [86]. Näistä kantasoluista käytetään termiä mesenkymaaliset kantasolut ja on epätodennäköistä, että niistä muodostuisi dopamiinisoluja. Ne saattavat vaikuttaa esimerkiksi immunologisten mekanismien tai hermokasvutekijöiden kautta, mutta vaaditaan lisätutkimuksia osoittamaan niiden mahdollinen hyöty Parkinsonin taudissa [87].
Vuonna 2015 dos. Filip Scheperjans kollegoineen Helsingin yliopistosta raportoi, että parkinsonpotilaiden ulosteiden mikrobiomikoostumus on erilainen kuin terveillä [88]. Tämä suomalainen tutkimus oli yksi ensimmäisistä, jossa tämä mikrobimuutos havaittiin. Tämän jälkeen monet tutkimusryhmät eri puolilta maailmaa ovat raportoineet monia erilaisia mikrobikoostumuksen muutoksia parkinsonpotilailla [89]. Toistaiseksi on epäselvää, mikä merkitys mikrobimuutoksilla on Parkinsonin taudin synnyssä ja etenemisessä, mutta tulokset ovat korostaneet suoliston merkitystä Parkinsonin taudissa. Esitettiin, että osalla potilaista Parkinsonin tauti alkaisi suolistosta (”gut first”) ja leviäisi sieltä hermostoon, mutta osalla tapahtuisi päinvastoin (”brain first”) [90].
Hoidoista mainittakoon apomorfiinin ihonalainen käyttö vaikeissa Parkinsonin oireissa [72]. Tämä hoito on ollut käytössä monissa Euroopan maissa jo 1990-luvulta lähtien, mutta Suomessa se sai viralliset hyväksynnät vasta v. 2013 (injektio) ja 2016 (infuusio). Sitä voidaan antaa jatkuvana infuusiona (Dacepton) tai yksittäisinä pistoksina ihon alle (Apogo Pen). Se vaikuttaa hyvin nopeasti, mutta vain noin tunnin verran yhden pistoksen jälkeen. Siihen voi liittyä myös pahoinvointia ja oksentelua ja sen käyttö vaatii usein pahoinvointilääkkeen käyttöä ainakin hoidon alussa. Vuonna 2020 USA:ssa hyväksyttiin käyttöön kielen alle laitettava liukeneva apomorfiinia sisältävä filmi (Kynmobi), joka on tarkoitettu äkillisiin OFF-vaiheisiin, kuten apomorfiinikynäkin [91]. Euroopassa tätä valmistetta ei toistaiseksi ole käytettävissä.
Levodopan inhaloitava valmiste (Inbrija) hyväksyttiin Parkinsonin taudin hoitoon v. 2018 USA:ssa ja v. 2019 EU:ssa [92]. Se on tarkoitettu käytettäväksi äkilliseen huonoon vaiheeseen (OFF-vaiheeseen) hengitysteihin inhaloiden. Sen vaikutus on hitaampi kuin apomorfiinipistoksen, mutta nopeampi kuin suun kautta otettavan levodopan [93]. Suomen markkinoille valmistetta ei ole toistaiseksi tuotu.
Vuonna 2018 USA:ssa hyväksyttiin talamukseen kohdennettu ultraäänihoito (HIFU) vapinan hoitoon (Parkinsonin tauti, essentiaalinen vapina) ja 2021 hoitokohteeksi hyväksyttiin myös globus pallidus-tumake Parkinsonin taudin motoristen oireiden hoitoon. Hoito otettiin käyttöön Turussa keväällä 2023. Tämän hoidon etuna on, ettei kalloa tarvitse avata, mutta toisaalta haittana on, että hoitoa voidaan käyttää vain yhdelle puolelle aivoa [94].
2010-luvulla korostettiin yhä enemmän liikunnan merkitystä Parkinsonin taudin oireiden hoidossa ja esitettiin, että sillä saattaisi olla jopa taudin etenemistä hidastavaa vaikutusta [95] ja että se pienentää riskiä sairastua Parkinsonin tautiin [96].
2010-luvulla tehtiin useammalla aineella tutkimuksia, joiden päämääränä oli hidastaa Parkinsonin taudin etenemistä. Valitettavasti tulokset jäivät näissä neuroprotektiivisissa tutkimuksissa negatiivisiksi. Tutkittavina aineina olivat mm. koentsyymi Q10 eli ubikinoni [97], kreatiini [98], kalsium-antagonisti isradipiini [99], uraattia kohottava inosiini [100] ja raudansitoja deferiproni [101]. Tällä hetkellä taudin etenemistä ehkäisevät tutkimukset keskittyvät erityisesti väärin laskostuneen alfa-synukleiinin kertymisen estoon, muta myös monia muita mekanismeja tutkitaan tiiviisti.
12. 2020-luku
Vuonna 2020 raportoitiin ensimmäiset hoitokokeilut dopamiinia muodostavilla kantasoluilla USA:ssa ja Japanissa [102, 103] ja 2020-luvun puolella mukaan on tullut useampia keskuksia [104]. Näissä tutkimuksissa käytetään yleensä ns. indusoituja monikykyisiä kantasoluja (iPSC), joiden alkuperänä voi olla esimerkiksi ihosolut ja jotka saadaan erilaistumaan dopamiinisoluiksi [105]. Toinen kantasolun lähde on alkiosta eristetyt solut eli ns. embryonaaliset kantasolut (ESC). Dopamiinia muodostavat solut ruiskutetaan yleensä molemmin puolin striatumiin. Laajempia tuloksia näiden kantasolusiirtojen hyödyistä ja haitoista potilailla ei ole vielä käytettävissä.
2020-luvun alkupuolella tuli käyttöön jälleen yksi uusi levodopan hoitomuoto, nimittäin levodopan ihonalainen infuusio pumpun avulla kahden eri lääketehtaan toimesta [106, 107]. Virallisesti valmisteita ei ole vielä hyväksytty käyttöön.
Loppusanat ja viitteet
Kaiken kaikkiaan Parkinsonin taudin historia on monivivahteinen ja osoittaa, että monet asiat keksitään ”uudelleen” vuosien kuluessa. Sekä potilaat että hoitavat lääkärit odottavat sitä historiallista päivää, kun joku keksii tähän tautiin parantavan tai edes taudin etenemistä estävän hoidon.
Artikkelin on toimittanut ja 1.9.2023 päivittänyt Seppo Kaakkola, prof.(h.c.), neurologian ja kliinisen farmakologian erikoislääkäri.
Viitteet
1. Gourie-Devi M, Ramu MG, Venkataram BS. Treatment of Parkinson’s disease in ’Ayurveda’ (ancient Indian system of medicine): discussion paper. J R Soc Med, 1991. 84(8): 491-2. https://doi.org/10.1177/014107689108400814
2. Manyam BV. Paralysis agitans and levodopa in ”Ayurveda”: ancient Indian medical treatise. Mov Disord, 1990. 5(1): 47-8. https://doi.org/10.1002/mds.870050112
3. Zhang ZX, Dong ZH, Roman GC. Early descriptions of Parkinson disease in ancient China. Arch Neurol, 2006. 63(5): 782-4. https://doi.org/10.1001/archneur.63.5.782
4. Zheng GQ. Therapeutic history of Parkinson’s disease in Chinese medical treatises. J Altern Complement Med, 2009. 15(11): 1223-30. https://doi.org/10.1089/acm.2009.0101
5. Koehler PJ, Keyser A. Tremor in Latin texts of Dutch physicians: 16th-18th centuries. Mov Disord, 1997. 12(5): 798-806. https://doi.org/10.1002/mds.870120531
6. Calne DB, Dubini A, Stern G. Did Leonardo describe Parkinson’s disease? N Engl J Med, 1989. 320(9): 594. https://doi.org/10.1056/NEJM198903023200912
7. Bereczki D. The description of all four cardinal signs of Parkinson’s disease in a Hungarian medical text published in 1690. Parkinsonism Relat Disord, 2010. 16(4): 290-3. https://doi.org/10.1016/j.parkreldis.2009.11.006
8. Stern G. Did parkinsonism occur before 1817? J Neurol Neurosurg Psychiatry, 1989. Suppl: 11-2. https://doi.org/10.1136/jnnp.52.suppl.11
9. Parkinson J, An Essay on the Shaking Palsy. 1817, London: Sherwood, Neely & Jones.
10. Pearce JM. Aspects of the history of Parkinson’s disease. J Neurol Neurosurg Psychiatry, 1989. Suppl: 6-10. https://doi.org/10.1136/jnnp.52.suppl.6
11. Goetz CG. Charcot on Parkinson’s disease. Mov Disord, 1986. 1(1): 27-32. https://doi.org/10.1002/mds.870010104
12. Barger G, Dale HH. Chemical structure and sympathomimetic action of amines. J Physiol, 1910. 41(1-2): 19-59. https://doi.org/10.1113/jphysiol.1910.sp001392
13. Lees AJ, Selikhova M, Andrade LA et al. The black stuff and Konstantin Nikolaevich Tretiakoff. Mov Disord, 2008. 23(6): 777-83. https://doi.org/10.1002/mds.21855
14. Holdorff B. Friedrich Heinrich Lewy (1885-1950) and his work. J Hist Neurosci, 2002. 11(1): 19-28. https://doi.org/10.1076/jhin.11.1.19.9106
15. Relander K. Patognomisia silmäänpistäviä tunnusmerkkejä muutamissa hermotaudeissa. Duodecim, 1890. 10: 165-170.
16. Krusz JC, Koller WC, Ziegler DK. Historical review: abnormal movements associated with epidemic encephalitis lethargica. Mov Disord, 1987. 2(3): 137-41. https://doi.org/10.1002/mds.870020301
17. Lunsford LD. Lars Leksell. Notes at the side of a raconteur. Stereotact Funct Neurosurg, 1996. 67(3-4): 153-68. https://doi.org/10.1159/000099445
18. Laitinen LV. Personal memories of the history of stereotactic neurosurgery. Neurosurgery, 2004. 55(6): 1420-8; discussion 1428-9. https://doi.org/10.1227/01.neu.0000143145.00880.f4
19. Quinn NP. Anti-parkinsonian drugs today. Drugs, 1984. 28(3): 236-62. https://doi.org/10.2165/00003495-198428030-00002
20. Talanti S. Parkinsonin tauti. Duodecim, 1963. 79: 570-578.
21. Barcroft H, Schwab RS. The effect of apomorphine and that of adrenalin, on the tremor of Parkinson’s disease. J Nerv Ment Dis, 1951. 114(6): 541-2.
22. Carlsson A, Lindqvist M, Magnusson T. 3,4-Dihydroxyphenylalanine and 5-hydroxytryptophan as reserpine antagonists. Nature, 1957. 180(4596): 1200. https://doi.org/10.1038/1801200a0
23. Carlsson A, Lindqvist M, Magnusson T et al. On the presence of 3-hydroxytyramine in brain. Science, 1958. 127(3296): 471. https://doi.org/10.1126/science.127.3296.471
24. Carlsson A. Treatment of Parkinson’s with L-DOPA. The early discovery phase, and a comment on current problems. J Neural Transm (Vienna), 2002. 109(5-6): 777-87. https://doi.org/10.1007/s007020200064
25. Ehringer H, Hornykiewicz O. Verteilung von Noradrenalin und Dopamin (3-Hydroxytyramin) im Gehirn des Menschen und ihr Verhalten bei Erkrankungen des Extrapyramidalen Systems. Klin Wochenschr, 1960. 38: 1236-9. https://doi.org/10.1007/BF01485901
26. Birkmayer W, Hornykiewicz O. Der l-Dioxyphenylalanin (l-Dopa)-Effekt bei der Parkinson-Akinese. Wien Klin Wochenschr, 1961. 73: 787-8.
27. Sano H. Biochemistry of the extrapyramidal system. Shinkei Kennkyu No Shinpo, Advances in Neurological Sciences. (ISSN 0001-8724) Tokyo, October 1960;5:42-48. Parkinsonism Relat Disord, 2000. 6(1): 3-6. https://doi.org/10.1016/s1353-8020(99)00046-2
28. Roe DL. From DOPA to Parkinson’s disease: the early history of dopamine research. J Hist Neurosci, 1997. 6(3): 291-301. https://doi.org/10.1080/09647049709525715
29. Hornykiewicz O. L-DOPA: from a biologically inactive amino acid to a successful therapeutic agent. Amino Acids, 2002. 23(1-3): 65-70. https://doi.org/10.1007/s00726-001-0111-9
30. Fahn S. The history of dopamine and levodopa in the treatment of Parkinson’s disease. Mov Disord, 2008. 23 Suppl 3: S497-508. https://doi.org/10.1002/mds.22028
31. Funk C. LXV.—Synthesis of dl-3: 4-Dihydroxyphenylalanine. J Chem Soc Trans, 1911. 99: 554-557.
32. Guggenheim M. Dioxyphenylalanin, eine neue Aminosäure aus Vicia faba. Hoppe-Seyler’s Z Physiol Chem, 1913. 88: 276-284.
33. Rinne UK, Sonninen V. A double blind study of l-dopa treatment in Parkinson’s disease. Eur Neurol, 1968. 1(3): 180-91. https://doi.org/10.1159/000113660
34. Cotzias GC, Van Woert MH, Schiffer LM. Aromatic amino acids and modification of parkinsonism. N Engl J Med, 1967. 276(7): 374-9. https://doi.org/10.1056/NEJM196702162760703
35. Cotzias GC. L-Dopa for Parkinsonism. N Engl J Med, 1968. 278(11): 630. https://doi.org/10.1056/nejm196803142781127
36. Yahr MD, Duvoisin RC, Schear MJ et al. Treatment of parkinsonism with levodopa. Arch Neurol, 1969. 21(4): 343-54. https://doi.org/10.1001/archneur.1969.00480160015001
37. Kivalo E, Boman K, Meurman T et al. L-dopa-hoito parkinsonismissa. Suomen Lääkäril, 1969. 24: 3198-3202.
38. Rinne UK. Levodopahoito Parkinsonin taudissa. Duodecim, 1971. 87(12): 929-932.
39. Schwab RS, England AC, Jr., Poskanzer DC et al. Amantadine in the treatment of Parkinson’s disease. JAMA, 1969. 208(7): 1168-70.
40. Hoehn MM, Yahr MD. Parkinsonism: onset, progression and mortality. Neurology, 1967. 17(5): 427-42. https://doi.org/10.1212/wnl.17.5.427
41. Pinder RM, Brogden RN, Sawyer PR et al. Levodopa and decarboxylase inhibitors: a review of their clinical pharmacology and use in the treatment of parkinsonism. Drugs, 1976. 11(5): 329-77. https://doi.org/10.2165/00003495-197611050-00001
42. Kebabian JW, Calne DB. Multiple receptors for dopamine. Nature, 1979. 277(5692): 93-6. https://doi.org/10.1038/277093a0
43. Calne DB, Teychenne PF, Claveria LE et al. Bromocriptine in Parkinsonism. Br Med J, 1974. 4(5942): 442-4. https://doi.org/10.1136/bmj.4.5942.442
44. Saarinen A, Myllylä V, Reunanen M et al. Bromokriptiini. Duodecim, 1977. 93(19): 1219-26.
45. Foley P, Gerlach M, Double KL et al. Dopamine receptor agonists in the therapy of Parkinson’s disease. J Neural Transm (Vienna), 2004. 111(10-11): 1375-446. https://doi.org/10.1007/s00702-003-0059-x
46. Davis GC, Williams AC, Markey SP et al. Chronic Parkinsonism secondary to intravenous injection of meperidine analogues. Psychiatry Res, 1979. 1(3): 249-54. https://doi.org/10.1016/0165-1781(79)90006-4
47. Langston JW, Ballard P, Tetrud JW et al. Chronic Parkinsonism in humans due to a product of meperidine-analog synthesis. Science, 1983. 219(4587): 979-80. https://doi.org/10.1126/science.6823561
48. Knoll J. The pharmacological profile of (-)deprenyl (selegiline) and its relevance for humans: a personal view. Pharmacol Toxicol, 1992. 70(5 Pt 1): 317-21. https://doi.org/10.1111/j.1600-0773.1992.tb00480.x
49. Oldfield V, Keating GM, Perry CM. Rasagiline: a review of its use in the management of Parkinson’s disease. Drugs, 2007. 67(12): 1725-47. https://doi.org/10.2165/00003495-200767120-00006
50. Deeks ED. Safinamide: first global approval. Drugs, 2015. 75(6): 705-11. https://doi.org/10.1007/s40265-015-0389-7
51. Marttila R, Heikkinen E, Hänninen J et al. Parkinsonin tauti. Duodecim, 2006. 122(21): 2655-6.
52. Garnett ES, Firnau G, Nahmias C. Dopamine visualized in the basal ganglia of living man. Nature, 1983. 305(5930): 137-8. https://doi.org/10.1038/305137a0
53. Garnett ES, Nahmias C, Firnau G. Central dopaminergic pathways in hemiparkinsonism examined by positron emission tomography. Can J Neurol Sci, 1984. 11(1 Suppl): 174-9. https://doi.org/10.1017/s0317167100046369
54. Ba F, Martin WR. Dopamine transporter imaging as a diagnostic tool for parkinsonism and related disorders in clinical practice. Parkinsonism Relat Disord, 2015. 21(2): 87-94. https://doi.org/10.1016/j.parkreldis.2014.11.007
55. Kokkonen A, Kaasinen V, Jutila L et al. PET aivosairauksissa. Duodecim, 2020. 136: 1110-7.
56. Männistö PT, Kaakkola S. Catechol-O-methyltransferase (COMT): biochemistry, molecular biology, pharmacology, and clinical efficacy of the new selective COMT inhibitors. Pharmacol Rev, 1999. 51(4): 593-628.
57. Kaakkola S. Clinical pharmacology, therapeutic use and potential of COMT inhibitors in Parkinson’s disease. Drugs, 2000. 59(6): 1233-50. https://doi.org/10.2165/00003495-200059060-00004
58. Teräväinen H. Entakaponi Parkinsonin taudin hoidossa. Duodecim, 1999. 115(24): 2734-44.
59. Rinne U, Ruottinen H, Gordin A. COMT-eston asema Parkinsonin taudin lääkehoidossa. Suomen Lääkäril, 2000. 55: 189-96.
60. Keating GM, Lyseng-Williamson KA. Tolcapone: a review of its use in the management of Parkinson’s disease. CNS Drugs, 2005. 19(2): 165-84. https://doi.org/10.2165/00023210-200519020-00006
61. Laitinen LV, Bergenheim AT, Hariz MI. Leksell’s posteroventral pallidotomy in the treatment of Parkinson’s disease. J Neurosurg, 1992. 76(1): 53-61. https://doi.org/10.3171/jns.1992.76.1.0053
62. Benabid AL, Benazzouz A, Hoffmann D et al. Long-term electrical inhibition of deep brain targets in movement disorders. Mov Disord, 1998. 13 Suppl 3: 119-25. https://doi.org/10.1002/mds.870131321
63. Heikkinen E, Erola T, Tuominen J et al. Parkinsonin taudin sähköstimulaatiohoito. Duodecim, 2004. 120(7): 789-96.
64. Merola A, Romagnolo A, Krishna V et al. Current Directions in Deep Brain Stimulation for Parkinson’s Disease-Directing Current to Maximize Clinical Benefit. Neurol Ther, 2020. 9(1): 25-41. https://doi.org/10.1007/s40120-020-00181-9
65. Madrazo I, Drucker-Colin R, Diaz V et al. Open microsurgical autograft of adrenal medulla to the right caudate nucleus in two patients with intractable Parkinson’s disease. N Engl J Med, 1987. 316(14): 831-4. https://doi.org/10.1056/NEJM198704023161402
66. Lindvall O. Stem cells for cell therapy in Parkinson’s disease. Pharmacol Res, 2003. 47(4): 279-87. https://doi.org/10.1016/s1043-6618(03)00037-9
67. Olanow CW, Kordower JH, Freeman TB. Fetal nigral transplantation as a therapy for Parkinson’s disease. Trends Neurosci, 1996. 19(3): 102-9. https://doi.org/10.1016/s0166-2236(96)80038-5
68. Freed CR, Greene PE, Breeze RE et al. Transplantation of embryonic dopamine neurons for severe Parkinson’s disease. N Engl J Med, 2001. 344(10): 710-9. https://doi.org/10.1056/NEJM200103083441002
69. Olanow CW, Goetz CG, Kordower JH et al. A double-blind controlled trial of bilateral fetal nigral transplantation in Parkinson’s disease. Ann Neurol, 2003. 54(3): 403-14. https://doi.org/10.1002/ana.10720
70. Polymeropoulos MH, Lavedan C, Leroy E et al. Mutation in the alpha-synuclein gene identified in families with Parkinson’s disease. Science, 1997. 276(5321): 2045-7. https://doi.org/10.1126/science.276.5321.2045
71. Spillantini MG, Schmidt ML, Lee VM et al. Alpha-synuclein in Lewy bodies. Nature, 1997. 388(6645): 839-40. https://doi.org/10.1038/42166
72. Guadagnolo D, Piane M, Torrisi MR et al. Genotype-Phenotype Correlations in Monogenic Parkinson Disease: A Review on Clinical and Molecular Findings. Front Neurol, 2021. 12: 648588. https://doi.org/10.3389/fneur.2021.648588
73. Li JL, Lin TY, Chen PL et al. Mitochondrial Function and Parkinson’s Disease: From the Perspective of the Electron Transport Chain. Front Mol Neurosci, 2021. 14: 797833. https://doi.org/10.3389/fnmol.2021.797833
74. Salamon A, Zadori D, Szpisjak L et al. Neuroprotection in Parkinson’s disease: facts and hopes. J Neural Transm (Vienna), 2020. 127(5): 821-829. https://doi.org/10.1007/s00702-019-02115-8
75. Braak H, Del Tredici K, Rub U et al. Staging of brain pathology related to sporadic Parkinson’s disease. Neurobiol Aging, 2003. 24(2): 197-211. https://doi.org/10.1016/s0197-4580(02)00065-9
76. Rietdijk CD, Perez-Pardo P, Garssen J et al. Exploring Braak’s Hypothesis of Parkinson’s Disease. Front Neurol, 2017. 8: 37. https://doi.org/10.3389/fneur.2017.00037
77. Chaudhuri KR, Healy DG, Schapira AH et al. Non-motor symptoms of Parkinson’s disease: diagnosis and management. Lancet Neurol, 2006. 5(3): 235-45. https://doi.org/10.1016/S1474-4422(06)70373-8
78. Weintraub D, Siderowf AD, Potenza MN et al. Association of dopamine agonist use with impulse control disorders in Parkinson disease. Arch Neurol, 2006. 63(7): 969-73. https://doi.org/10.1001/archneur.63.7.969
79. Joutsa J, Kaasinen V. Parkinsonin taudin impulssikontrollihäiriöt. Duodecim, 2013. 129(22): 2351-8.
80. Nyholm D. Pharmacokinetic optimisation in the treatment of Parkinson’s disease : an update. Clin Pharmacokinet, 2006. 45(2): 109-36. https://doi.org/10.2165/00003088-200645020-00001
81. Pekkonen E. Levodopainfuusio ja apomorfiini Parkinsonin taudin hoidossa. Duodecim, 2008. 124(4): 402-9.
82. Nyholm D, Jost WH. Levodopa-entacapone-carbidopa intestinal gel infusion in advanced Parkinson’s disease: real-world experience and practical guidance. Ther Adv Neurol Disord, 2022. 15: 17562864221108018. https://doi.org/10.1177/17562864221108018
83. Gill SS, Patel NK, Hotton GR et al. Direct brain infusion of glial cell line-derived neurotrophic factor in Parkinson disease. Nat Med, 2003. 9(5): 589-95. https://doi.org/10.1038/nm850
84. Lang AE, Gill S, Patel NK et al. Randomized controlled trial of intraputamenal glial cell line-derived neurotrophic factor infusion in Parkinson disease. Ann Neurol, 2006. 59(3): 459-66. https://doi.org/10.1002/ana.20737
85. Huttunen H, Booms S, Sjögren M et al. First-in-man clinical trial of intraputamenal CDNF in Parkinson’s disease finds a consorted biomarker response in a subgroup of subjects. Mov Disord, 2021. 36 (suppl 1).
86. Venkataramana NK, Kumar SK, Balaraju S et al. Open-labeled study of unilateral autologous bone-marrow-derived mesenchymal stem cell transplantation in Parkinson’s disease. Transl Res, 2010. 155(2): 62-70. https://doi.org/10.1016/j.trsl.2009.07.006
87. Fricova D, Korchak JA, Zubair AC. Challenges and translational considerations of mesenchymal stem/stromal cell therapy for Parkinson’s disease. NPJ Regen Med, 2020. 5(1): 20. https://doi.org/10.1038/s41536-020-00106-y
88. Scheperjans F, Aho V, Pereira PA et al. Gut microbiota are related to Parkinson’s disease and clinical phenotype. Mov Disord, 2015. 30(3): 350-8. https://doi.org/10.1002/mds.26069
89. Kleine Bardenhorst S, Cereda E, Severgnini M et al. Gut microbiota dysbiosis in Parkinson disease: A systematic review and pooled analysis. Eur J Neurol, 2023. https://doi.org/10.1111/ene.15671
90. Borghammer P, Van Den Berge N. Brain-First versus Gut-First Parkinson’s Disease: A Hypothesis. J Parkinsons Dis, 2019. 9(s2): S281-S295. https://doi.org/10.3233/JPD-191721
91. Caughman CY, Factor S. A critical review of apomorphine hydrochloride sublingual film for the treatment of Parkinson’s disease ’OFF’ episodes. Expert Rev Neurother, 2021. 21(2): 169-177. https://doi.org/10.1080/14737175.2020.1855145
92. Hauser RA, LeWitt PA, Waters CH et al. The Clinical Development of Levodopa Inhalation Powder. Clin Neuropharmacol, 2023. 46(2): 66-78. https://doi.org/10.1097/WNF.0000000000000540
93. Martinez-Nunez AE, LeWitt PA. Drugs to the Rescue: Comparison of On-Demand Therapies for OFF Symptoms in Parkinson’s Disease. J Parkinsons Dis, 2023. https://doi.org/10.3233/JPD-230055
94. Brück A, Sequeiros R, Frantzén J et al. Kohdennettu ultraääni vapinan hoidossa. Duodecim, 2023. 139(9): 713-720.
95. Mak MKY, Wong-Yu ISK. Exercise for Parkinson’s disease. Int Rev Neurobiol, 2019. 147: 1-44. https://doi.org/10.1016/bs.irn.2019.06.001
96. Fang X, Han D, Cheng Q et al. Association of Levels of Physical Activity With Risk of Parkinson Disease: A Systematic Review and Meta-analysis. JAMA Netw Open, 2018. 1(5): e182421. https://doi.org/10.1001/jamanetworkopen.2018.2421
97. Parkinson Study Group QEI, Beal MF, Oakes D et al. A randomized clinical trial of high-dosage coenzyme Q10 in early Parkinson disease: no evidence of benefit. JAMA Neurol, 2014. 71(5): 543-52. https://doi.org/10.1001/jamaneurol.2014.131
98. Writing Group for the NETiPDI, Kieburtz K, Tilley BC et al. Effect of creatine monohydrate on clinical progression in patients with Parkinson disease: a randomized clinical trial. JAMA, 2015. 313(6): 584-93. https://doi.org/10.1001/jama.2015.120
99. Parkinson Study Group S-PDIIII. Isradipine Versus Placebo in Early Parkinson Disease: A Randomized Trial. Ann Intern Med, 2020. 172(9): 591-598. https://doi.org/10.7326/M19-2534
100. Parkinson Study Group S-PDI, Schwarzschild MA, Ascherio A et al. Effect of Urate-Elevating Inosine on Early Parkinson Disease Progression: The SURE-PD3 Randomized Clinical Trial. JAMA, 2021. 326(10): 926-939. https://doi.org/10.1001/jama.2021.10207
101. Devos D, Labreuche J, Rascol O et al. Trial of Deferiprone in Parkinson’s Disease. N Engl J Med, 2022. 387(22): 2045-2055. https://doi.org/10.1056/NEJMoa2209254
102. Takahashi J. iPS cell-based therapy for Parkinson’s disease: A Kyoto trial. Regen Ther, 2020. 13: 18-22. https://doi.org/10.1016/j.reth.2020.06.002
103. Schweitzer JS, Song B, Herrington TM et al. Personalized iPSC-Derived Dopamine Progenitor Cells for Parkinson’s Disease. N Engl J Med, 2020. 382(20): 1926-1932. https://doi.org/10.1056/NEJMoa1915872
104. Cha Y, Park TY, Leblanc P et al. Current Status and Future Perspectives on Stem Cell-Based Therapies for Parkinson’s Disease. J Mov Disord, 2023. 16(1): 22-41. https://doi.org/10.14802/jmd.22141
105. Weltner J, Trokovic R, Otonkoski T. Indusoidut pluripotentit kantasolut lääketieteellisessä tutkimuksessa. Duodecim, 2014. 130(8): 785-92.
106. Soileau MJ, Aldred J, Budur K et al. Safety and efficacy of continuous subcutaneous foslevodopa-foscarbidopa in patients with advanced Parkinson’s disease: a randomised, double-blind, active-controlled, phase 3 trial. Lancet Neurol, 2022. 21(12): 1099-1109. https://doi.org/10.1016/S1474-4422(22)00400-8
107. Giladi N, Gurevich T, Djaldetti R et al. ND0612 (levodopa/carbidopa for subcutaneous infusion) in patients with Parkinson’s disease and motor response fluctuations: A randomized, placebo-controlled phase 2 study. Parkinsonism Relat Disord, 2021. 91: 139-145. https://doi.org/10.1016/j.parkreldis.2021.09.024