Finska humanstudier kring rörelsestörningar år 2023
I 2023 års publikationsdatabaser finns 47 internationella publikationer som har uteslutande eller huvudsakligen finska upphovspersoner och som redogör för forskning med koppling till rörelsestörningssjukdomar (patientundersökningar eller andra humanstudier). Antalet har förblivit nästan oförändrat jämfört med år 2022.
Cirka 65 % av studierna rör Parkinsons sjukdom eller andra parkinsonismer. Andelen är mindre än tidigare och detta betyder att också andra rörelsestörningssjukdomar är föremål för forskning i Finland. Publikationerna handlar om dystoni, ataxi, Hungtingtons sjukdom, Wilsons sjukdom samt Tourettes syndrom. Några publikationer behandlar tremor, ett ämne som inte förekommit på många år. De vanligaste forskningsområdena rörde registerstudier, avbildning och ärftliga faktorer. Geografiskt genomfördes de flesta studier vid Helsingfors och Åbo universitet och universitetssjukhus knutna till dessa lärosäten, men även andra universitet (Kuopio, Uleåborg och Tammerfors) har publicerat flera studier.
Innehållsförteckning
- Parkinsons sjukdom, epidemiologi
- Parkinsons sjukdom, avbildning
- Parkinsons sjukdom, läkemedelsundersökningar
- Parkinsons sjukdom, djup hjärnstimulering (DBS)
- Parkinsons sjukdom, genetik
- Parkinsons sjukdom, mikrober
- Parkinsons sjukdom, dyskinesier
- Parkinsons sjukdom, tal
- Parkinsons sjukdom, smarta enheter
- Parkinsons sjukdom, kliniskt test
- Parkinsons sjukdom, egenvård
- Lewykroppsdemens
- Dystoni/Dyskinesi
- Ataxi
- Tremor
- Huntingtons sjukdom
- Wilsons sjukdom
- Tourettes syndrom
- Neuroepidemiologi
- Hemifacial spasm
Parkinsons sjukdom, epidemiologi
Anna-Maija Tolppanen, professor vid Östra Finlands universitet, publicerade tillsammans med sin forskningsgrupp fem studier där man utrett sambandet mellan användning av vissa läkemedel eller annan exponering och uppkomst av Parkinsons sjukdom. Samtliga studier utgick från finska registerdata (bland annat FPA, THL, Finlands Cancerregister, Statistikcentralen och Befolkningsregistercentralen). Databasen över parkinsonpatienter bygger på patientdata som samlats in inom ramen för forskningsprojektet FINPARK.
I den första studien konstaterade gruppen att det inte finns något säkert samband mellan astmaläkemedel som vidgar luftrören (beta-agonister) och uppkomst av Parkinsons sjukdom [1]. Detta resultat skiljer sig från resultat av vissa andra studier där man funnit att astmaläkemedel minskar risken för Parkinsons sjukdom. Den finska studiens styrka ligger i att det finns goda registeruppgifter och att man beaktar förväxlingsfaktorer.
I sin andra studie tog gruppen reda på huruvida det hos parkinsonpatienter finns ett samband mellan inledande av behandling med antipsykotiska läkemedel och att bli intagen på sjukhus [2]. Patienterna i studien får antipsykotiska läkemedel (såsom kvetiapin, risperidon och klozapin) mot hallucinationer och andra psykotiska symptom. Gruppen fann ett klart samband mellan användning av antipsykotiska läkemedel och behov av sjukhusvård. Vistelsen på sjukhuset var också längre hos patienter som använde antipsykotika. Fyndet torde säga oss att parkinsonpatienters neuropsykiatriska symptom ofta kräver sjukhusvård, och att inledandet av medicineringen inte i sig förorsakar behovet av sjukhusvård.
I sin tredje undersökning utredde man parkinsonpatienters användning av hjärt- och blodtrycksmediciner och antikoagulanter (s.k. blodförtunnande läkemedel) [3]. Innan de fått diagnosen Parkinsons sjukdom använde patienterna i något större utsträckning hjärt- och blodtrycksmediciner och antikoagulanter, men efter insjuknandet minskade användningen av hjärt- och blodtrycksmediciner. Av hjärtmedicinerna var den vanligaste gruppen betablockerare, som kan användas bland annat för att behandla tremor. Parkinsons sjukdom kan sänka blodtrycket (särskilt när patienten står upp) och detta kan vara orsaken till den minskade användningen av hjärt- och blodtrycksmediciner.
I en fjärde undersökning utreddes förekomsten av skador i huvudet hos parkinsonpatienter [4]. Parkinsons sjukdom medför fler fallolyckor och då är det rimligt att anta att antalet skador i huvudet också ökar. Detta kunde också konstateras utgående från det finska forskningsunderlaget. Parkinsons sjukdom mer än fördubblade risken för skador i huvudet, och medförde en nästan fördubblad risk för allvarliga hjärnskador. Dödligheten kopplad till sådana skador ökade också. Studien visar att åtgärder för att förebygga fallolyckor är ytterst viktiga vid Parkinsons sjukdom.
I sin femte studie utredde gruppen sambanden mellan exponering för partiklar i luften och uppkomst av Parkinsons sjukdom [5]. Man fann inget säkert samband mellan exponering för partikelföroreningar och risk för Parkinsons sjukdom. Studien utgår från finska förhållanden, vilka inte nödvändigtvis säger något om situationen globalt.
Forskare på Arbetshälsoinstitutet har studerat sambandet mellan exponering för lösningsmedel och risken att drabbas av Parkinsons sjukdom [6]. Flera tidigare studier har visat att exponering för lösningsmedel ökar risken för Parkinsons sjukdom. Särskilt trikloretylen (TCE) har varit på tapeten. I denna finska registerbaserade studie befanns exponering för lösningsmedel i någon mån öka risken för att insjukna i Parkinsons sjukdom, dock var riskökningen inte statistiskt signifikant. Rökning befanns minska risken, vilket också observerats i många tidigare studier. Exponeringsnivåerna i Finland är sannolikt ganska låga, och detta bidrar möjligen till att förklara att olika studier gett olika resultat. I undersökningar av detta slag förekommer många förväxlingsfaktorer som de finska forskarna strävar efter att ta i beaktande.
Docent Jussi Sipilä (Joensuu, Åbo) med kollegor undersökte dödligheten bland finska parkinsonpatienter [7]. Forskningsdata utgjordes av uppgifter om patienter som under perioden 2004–2018 diagnostiserats med Parkinsons sjukdom (23 688 patienter), utgående från FPA:s statistik över läkemedelsersättningar. Dessa patienter jämfördes med en slumpmässigt utvald kontrollgrupp (94 752 personer) med matchande ålders- och könsfördelning. Forskarna fann att finska parkinsonpatienter har mer än dubbelt så stor dödlighetsrisk i jämförelse med kontrollgruppen (bild 1). Mest hade dödligheten ökat bland patienter som insjuknat i yngre ålder. De vanligaste dödsorsakerna var grundsjukdomen (Parkinsons sjukdom), hjärt- och kärlsjukdomar samt cancersjukdomar. Studien visar att Parkinsons sjukdom alltjämt är förenad med ökad dödlighet, visserligen har riskökningen i många utländska studier visat sig vara något mindre.

Bild 1. Parkinsonpatienters överlevnad i jämförelse med kontrollpersoner(Survival of patients with Parkinson’s disease and age-, and sex-matched control subjects. Follow-up started at diagnosis of Parkinson’s disease. Dashed lines represent 95 % confidence intervals). Ur publikationen Sipilä m.fl. 2023 [7].
Parkinsons sjukdom, avbildning
Professor Valtteri Kaasinens forskningsgrupp från Åbo hittade ett samband mellan tidig förtvining (atrofi) av hjärnbarken och depression hos parkinsonpatienter [8]*. Studien omfattade 50 avlidna patienter (varav 30 lidit av Parkinsons sjukdom, 10 av progressiv supranukleär pares [PSP] och 10 av multipel systematrofi [MSA]). Diagnoserna hade fastställts genom neuropatologiska undersökningar. Alla patienter hade under sin levnad en eller två gånger genomgått en datortomografiundersökning av hjärnan för bedömning av hjärnbarkens tjocklek. Bedömningar om depression gjordes utifrån patienternas journaler. Forskarna konstaterade att i synnerhet atrofi av tinningloben var tydligare hos parkinsonpatienter med depression, och att också förtviningen av hjärnbarken hade ett snabbare förlopp hos dessa. Det är utifrån studien inte möjligt att avgöra vad som är orsak och vad som är verkan; dvs. får depressionen hjärnan att förtvina eller leder förtviningen av hjärnan till depression? Liknande fynd har gjorts också hos andra depressionspatienter.
Doktoranden Imran Waggan ur professor Juha Rinnes forskningsgrupp i Åbo publicerade två studier med PET-undersökningar av hjärnan. Som spårämne vid undersökningarna användes föreningen ([11C]TMSX) som fäster vid hjärnans A2A-adenosinreceptorer. Även bland annat koffein fäster vid dessa receptorer. I den första studien ingick 18 parkinsonpatienter och 7 kontrollpersoner [9]*. Forskarna fann att antalet A2A-adenosinreceptorer ökat i pann- och hjässlobens vita substans, men minskat i gråa substansen i syncentrum. I den andra studien ingick 9 parkinsonpatienter i ett tidigt skede av sjukdomen och 9 i ett mellanliggande skede samt 6 friska kontrollpersoner [10]*. Forskarna konstaterade att antalet A2A-adenosinreceptorer hos parkinsonpatienterna minskat i svanskärnan (caudatus-kärnan) och ökat i bleka kärnan. Dessa två studier räknas främst som grundforskning, och det återstår att se i vilken mån de får praktisk betydelse.
I en studie genomförd av neurologer från Helsingfors och Åbo utreddes sambanden mellan parkinsonpatienters tarmsymptom och förändringar i hjärnans dopamintransportörer [11]. Dopamintransportörer studeras genom en isotopundersökning (Spect-undersökning) som indirekt mäter antalet dopaminbanor i olika delar av hjärnan. I studien deltog 90 parkinsonpatienter som fick genomgå en Spect-undersökning. Därtill genomgick de en klinisk bedömning och besvarade olika slags enkäter om tarmsymptom. Inom ramen för studien hittades 17 patienter som uppfyllde kriterierna för irritabel tarmsyndrom (IBS). Dessa patienter hade ökad transportörbindning i den högra skalkärnan (putamen) och omgivande områden. Studien visar för sin del att det finns samband mellan förändringar i hjärnan och tarmbesvär, även om frågan om den exakta betydelsen av detta förblir obesvarad.
Professor Juho Joutsa från Åbo deltog i en internationell översiktsartikel där man gick igenom avbildningsstudier som publicerats om parkinsonismer (totalt 44 591 studier). För en slutlig utvärdering återstod 132 studier med magnet- (MRI-), PET- och Spect-bilddata [12]. Forskarna gjorde ett sammandrag av de typiska hjärnförändringar som observeras vid Parkinsons sjukdom, progressiv supranukleär pares (PSP), kortikobasal degeneration (CBD) och multipel systematrofi (MSA). Dessa data är till nytta särskilt för neurologer som behandlar rörelsestörningssjukdomar samt radiologer och isotopläkare som tolkar avbildningar.
Forskare från Åbo klargjorde vilka platser som skulle lämpa sig bäst för placering av elektroder vid EEG-undersökningar (elektroencefalografi) för upptäckt av tidig Parkinsons sjukdom [13]. Man studerade EEG-registreringar av såväl finska som amerikanska patienter. Forskarna kom fram till att ett begränsat antal elektroder (fem kanaler) ger tillräckligt tillförlitliga data. Det återstår att se om metoden möjliggör tillräckligt tillförlitlig screening av patienter i ett tidigt skede av sjukdomen.
Parkinsons sjukdom, läkemedelsundersökningar
Finska och svenska neurologer och neurokirurger publicerade tillsammans med forskare från Herantis Pharma resultat av en patientundersökning om nervtillväxtfaktorn CDNF [14]. CDNF (Cerebral dopamine neurotrophic factor) är en nervtillväxtfaktor som upptäckts av professor Mart Saarmas forskningsgrupp och som gett lovande resultat i djurmodeller av Parkinsons sjukdom. Herantis Pharma är ett finskt läkemedelsutvecklingsföretag, vars forskare tillsammans med finska, svenska och brittiska neurologer och neurokirurger planerade den första CDNF-studien på patienter. Eftersom CDNF ges direkt i hjärnvävnaden rör det sig om en tämligen komplicerad administreringsmetod där ett permanent rörsystem installeras i skallen och används för att injicera CDNF en gång i månaden. Under de första sex månaderna gavs patienterna antingen placebo eller två olika stora doser av CDNF. Under följande sexmånadersperiod fick alla patienter CDNF. I studien deltog 17 patienter. Injektionen av CDNF lyckades och orsakade ingen betydande skada. I anknytning till infusionsutrustningen utvecklades två varhärdar i hjärnan, dessa åtgärdades dock framgångsrikt när utrustningen avlägsnades. Ingen säkerställd förbättring konstaterades i patienternas mående, men hos enstaka patienter gav PET-undersökningen indikationer på positivt svar. Detta var en ambitiös studie som krävde mycket av både forskare och patienter. Man hade givetvis önskat bättre kliniska resultat, men å andra sidan är dessa resultat ganska lika de som tidigare erhållits med andra nervtillväxtfaktorer. Herantis Pharma ser nu ut att fokusera på en förening som skulle ha nervtillväxtfaktorns egenskaper men vara enklare att administrera (https://herantis.com/fi/(du kommer att omdirigeras till en annan tjänst)).
Läkemedelsbolaget Orions forskare publicerade en studie där de utredde hur höjning av dosen karbidopa påverkar plasmanivåer av levodopa [15]. I studien deltog 25 friska försökspersoner som fick en höjd dos av karbidopa (50 eller 100 mg) tillsammans med en tablett levodopa/karbidopa (100/25 mg). En del fick även entakapon (200 mg). Den ökade karbidopadosen höjde avsevärt plasmanivån av levodopa, särskilt i den grupp patienter som fått entakapon. Studien visar att det skulle vara klokt att öka mängden karbidopa i levodopa- och levodopa/entakapon-tabletter, men det torde kräva ytterligare patientundersökningar, något som läkemedelstillverkarna tills vidare inte är villiga att genomföra.
Neurologer vid Helsingfors universitet publicerade terapeutiska resultat avseende patienter som vårdats vid HUS neurologiska klinik och som fått levodopa/entakapon/karbidopa genom tarminfusion (Lecigon®) [16]*. Lecigon är ett nyare levodopapreparat som administreras som infusion i tarmen. I jämförelse med Duodopa®, som kommit ut tidigare på marknaden, innehåller Lecigon även entakapon. Den pump som behövs för infusion är också mindre än för Duodopa. Forskarna behandlade 30 patienter med Lecigon. Efter en uppföljningstid på sex månader avbröt sju av patienterna behandlingen, i huvudsak på grund av svårigheter med att komma fram till rätt dos eller av neuropsykiatriska skäl. De skador som rapporterats under behandlingen liknade de som rapporterats under behandling med Duodopa. Patienterna var nöjda med den lilla pumpen, som lär vara den mest uppenbara fördelen med detta nya preparat.
Parkinsons sjukdom, djup hjärnstimulering (DBS)
Neurologer och neurokirurger i Uleåborg publicerade två studier kring djup hjärnstimulering (DBS). I den första utredde forskarna subtalamiska kärnans kopplingar till de motoriska områdena i framloben (pars distalis), med hjälp av magnetavbildningar och analyser av nervbanor (traktografi) som gjorts utifrån dem [17]. (Subtalamiska kärnan är den plats där elektroder för stimulering oftast implanteras hos parkinsonpatienter.) Forskarna undersökte 22 stimulationspatienters patientuppgifter och MR-bilder. På grundval av resultaten bedömde de att stimulering av den del av subtalamiska kärnan som har direkt förbindelse med främre delen av supplementära motorbarken (presupplementära motorbarken) ger det bästa terapeutiska resultatet.
I den andra undersökningen studerades 43 parkinsonpatienters livskvalitet före stimulering av subtalamiska kärnan och ett år efter behandlingen [18]. Forskarna observerade att DBS-behandlingen förbättrade patienternas livskvalitet avsevärt, och även förbättrade motoriken och betydligt minskade behovet av läkemedelsbehandling (bild 2). Resultaten stöder tidigare observationer, men i fråga om livskvalitet finns få tidigare studier. I bild 2 presenteras deras studie grafiskt.
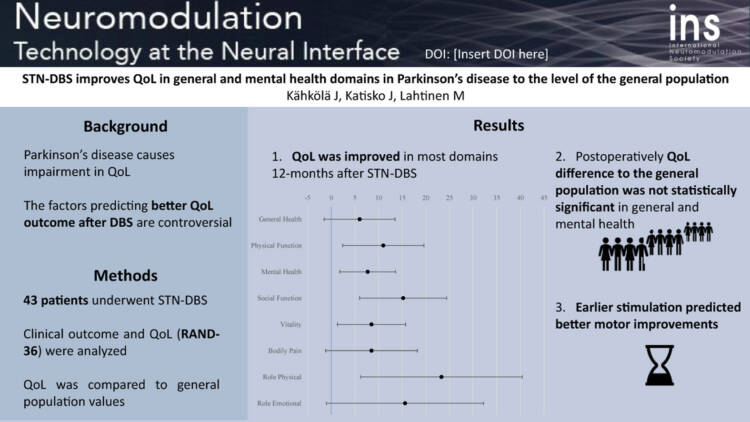
Bild 2. Den gynnsamma effekten av stimulering av subtalamiska kärnan på parkinsonpatienters livskvalitet. Ur publikationen Kähkölä m.fl. 2023 [18].
Parkinsons sjukdom, genetik
I en översiktsartikel beskrivs skapandet av nätverk mellan 59 forskningscenter runt om i världen som studerar Parkinsons sjukdom [19]. Från Finland deltog Åbo universitet, under ledning av professor Valtteri Kaasinen. Målet är att korrelera data särskilt i fråga om ärftliga former av Parkinsons sjukdom, eftersom enskilda forskningscentrum sällan har många patienter med sådana sjukdomsformer. Fint att Åbo redan deltar i detta.
Forskare från Uleåborg beskriver tre finska patienter som drabbats av Parkinsons sjukdom i tidig ålder (<50 år) och som befanns bära på en mutation på RFC1-genen [20]*. Det var känt sedan tidigare att mutationer på denna gen förorsakar en sjukdom som beskrivs som CANVAS-syndromet, vilket innebär degeneration av lillhjärnan och därpå följande ataxi, samt degeneration av balansorganet och degeneration av perifera nervsystemet (neuropati). Detta är en av de sällsynta genetiska defekter som hittats hos finska parkinsonpatienter.
Parkinsons sjukdom, mikrober
År 2023 publicerades endast en studie, delvis kopplad till Finland, kring sambanden mellan tarmbakterier och Parkinsons sjukdom. Det är klart färre än under de föregående åren. Docent Filip Scheperjans vid Helsingfors universitet var involverad i en internationell översiktsartikel där man behandlade tarmmikrobers betydelse för uppkomsten av Parkinsons sjukdom [21]. I översikten har man gått igenom publicerade studier kring detta ämne och sammanfattat resultaten. En närmare bedömning av artikeln kräver ansenliga kunskaper inom bakteriologi, men författarna drog slutsatsen att bakteriegrupper som bildar smörsyra har minskat hos parkinsonpatienter, medan bakteriegrupper som bryter ner slem har ökat. Detta skulle kunna leda till ökad inflammatorisk reaktion i tarmväggen.
Parkinsons sjukdom, dyskinesier
Professor Valtteri Kaasinen från Åbo medverkade i en internationell översiktsartikel där man bedömde kulturskillnader i fråga om hur parkinsonpatienter upplever den olägenhet som orsakas av tvångsmässiga rörelser av kroppen eller en kroppsdel (dyskinesier) [22]. I studien användes dyskinesi-data som samlats in av den internationella föreningen för Parkinsons sjukdom och rörelsestörningar (MDS). MDS har tagit fram en skala i flera punkter för utvärdering av dyskinesi, vilken översatts till åtminstone 16 olika språk. Analysen visade att det finns tydliga skillnader mellan språkområden (medborgarskap) i hur patienterna bedömde olägenheten av sina dyskinesier. Kinesisktalande var den grupp som upplevde dyskinesierna mest besvärande, medan koreansktalande i jämförelse med talare av andra språk upplevde dem som mindre besvärande. I fråga om finsktalande patienter konstaterades att resultatet låg nära genomsnittet. Studien visar att kulturskillnader i hög grad kan påverka utfallet av olika slags enkätundersökningar.
Parkinsons sjukdom, tal
Docent Nelly Penttilä från Tammerfors med kollegor publicerade två studier där man analyserat parkinsonpatienters tal. I den första studien deltog 31 parkinsonpatienter och 36 kontrollpersoner, vilkas inspelade tal analyserades med halvautomatiska metoder [23]. Forskarna observerade att de manliga patienternas tal (prosodi) skilde sig från kontrollpersonernas. I den andra studien testade forskarna automatisk analys av artikulation av vokaler i tal och jämförde resultaten med utvärderingar som gjorts genom lyssning [24]. I utvärderingen deltog 15 parkinsonpatienter och 15 kontrollpersoner. Resultatet visade att den automatiska metoden och den äldre lyssningsmetoden korrelerade och att den nya metoden möjligen lämpar sig för bedömning av talets begriplighet.
Parkinsons sjukdom, smarta enheter
Smarttelefoner och olika slags armband används i allt högre grad också för att bedöma symptom vid Parkinsons sjukdom. I en finsk multicenterstudie deltog 42 parkinsonpatienter och 23 kontrollpersoner. De fick bära ett smartarmband (Garmin Vivosmart 4) i fyra veckors tid och föra anteckningar om sitt mående och sin medicinering i en mobilapp [25]. I denna studie låg fokus särskilt på metoder för analys av rörelsedata från armbanden. Slutsatsen var att det behövs ytterligare studier för att system av detta slag ska ge tillförlitlig information.
Parkinsons sjukdom, kliniskt test
Ett typiskt drag hos parkinsonpatienter är mikrografi, dvs. att skriften vartefter krymper när personen skriver för hand. När man bett parkinsonpatienter att rita ett hus med fönster och ytterdörr har man konstaterat att patienten ofta inte klarar av att rita dörren ända ner till golvet. Fenomenet har kallats ”floating door sign” (bild 3) och ansetts vara ett typiskt drag för mikrografi vid Parkinsons sjukdom. Nu ville de finska neurologerna ta reda på hur specifikt detta fynd är för Parkinsons sjukdom [26]. I studien inkluderades 144 parkinsonpatienter och 41 patienter med essentiell tremor samt 38 friska kontrollpersoner. Resultatet var positivt hos 47 % av parkinsonpatienterna och 37 % av patienterna med essentiell tremor. Skillnaden var inte statistiskt signifikant. Det finns alltså orsak att överge detta test för påvisning av Parkinsons sjukdom.
Bild 3. Till vänster en normal teckning av ett hus, och till höger ett hus med en ”flytande dörr”.
Parkinsons sjukdom, egenvård
Forskare från Uleåborg medverkade i en studie som syftade till att erhålla information om parkinsonpatienters egenvårdsmetoder [27]. Det är välkänt att patienter ofta hittar på och utvecklar metoder för att må bättre i vardagen. Forskarna tog fram ett nätbaserat program som testades på 288 patienter och 31 närståendevårdare. Programmet är offentligt och tillgängligt för alla på en engelskspråkig webbplats (https://PDCareBox.com(du kommer att omdirigeras till en annan tjänst)). Jag rekommenderar alla att läsa mer om programmet.
Lewykroppsdemens
Om Lewykroppsdemens, alltså en minnessjukdom som förknippas med bland annat parkinsonismer och hallucinationer, publicerades två registerbaserade studier där psykiatrer verksamma i Helsingfors undersökte betydelsen av denna sjukdom för människors kriminella, dvs. brottsliga, beteende. Minnessjukdomar (Alzheimers sjukdom, degeneration i pann- och tinningloberna och Lewykroppsdemens) påverkar människans beteende och det är därför tänkbart att de skulle kunna öka benägenheten att begå förbrytelser eller brott. Att döma av registeruppgifterna ser detta dock inte ut att vara fallet åtminstone hos finska minnessjuka [28]. Antalet brott var ungefär hälften så stort som det förväntade antalet. De patienter som i störst utsträckning gör sig skyldiga till förbrytelser är manliga patienter med degeneration i pann- och tinningloberna och Lewykroppsdemens. I gruppens andra registerstudie utreddes dödligheten hos minnessjuka som dömts för förbrytelser eller brott [29]. Forskarna konstaterade att dödligheten var högre bland patienter med Lewykroppsdemens och kvinnliga patienter med degeneration i pann- och tinningloberna än bland referensbefolkningen utan brottslig bakgrund. Man lyckades inte utifrån registeruppgifterna dra några slutsatser om de exakta orsakerna bakom detta fynd.
Den helsingforsbördige forskaren MD Karri Kaivola, nu verksam i USA, var första författare till en omfattande studie där man utredde ärftliga avvikelser vid Lewykroppsdemens och degeneration i pann- och tinningloberna [30]. Forskarna gjorde en sekvensering av hela genomet för över 5 000 patientfall och över 4 000 kontrollpersoner. De hittade en ny deletion i TPCN1-genen, vilket ser ut att innebära en risk för Lewykroppsdemens. Därtill hittades nya varianter i gener med koppling till degeneration i pann- och tinningloberna. Småningom ökar kunskaperna kring gener och Lewykroppsdemens.
Docent Jussi Sipilä från universiteten i Joensuu och Åbo, tillsammans med kollegor från Uleåborg, hittade en finsk släkt där det fanns ett samband mellan en defekt på glukocerebrosidas-genen och snabbt framåtskridande Lewykroppsdemens [31]*. Det är känt sedan tidigare att olika variationer i glucocerebrosidas-genen (GBA1) ökar risken att drabbas av Parkinsons sjukdom eller Lewykroppsdemens. Forskarna beskrev två syskon som led av parkinsonismer och vilkas neuropatologiska fynd stämde in på Lewykroppsdemens. Hos båda påträffades en heterozygot variant av genen GBA1 (p.Pro454Leu). Det var känt att det i släkten tidigare funnits andra parkinsonpatienter som sannolikt burit på samma genvariant. Fyndet är ett tillägg till genetiska defekter hos finska parkinsonpatienter. Sådana defekter är tills vidare ganska få.
Dystoni/Dyskinesi
Professor Juho Joutsas forskningsgrupp från Åbo tog reda på hurdana ämnesomsättningsmässiga förändringar elektrisk stimulering av globus pallidus-kärnan (pallidum-kärnan) får till stånd i hjärnan [32]. Djup hjärnstimulering (DBS) av denna kärna används numera för att behandla svår cervikal dystoni. Det är dock inte känt varför behandlingen har effekt. I undersökningen deltog elva dystonipatienter som genomgick en PET-undersökning med fludeoxiglukose som mäter ämnesomsättningen. Undersökningen gjordes två gånger; utan och med stimulering. Stimuleringen ökade ämnesomsättningen i pallidum- och putamen-kärnorna, i subtalamiska kärnan och i primära områden i känsel- och motorbarken. Lindringen av dystonin korrelerade med förändringar i primära känsel- och motorbarken. Studien ger ny information om vilka nervnät som aktiveras av stimulering av pallidum-kärnan.
Professor Juho Joutsa var en av författarna till en omfattande översiktsartikel där man gick igenom avbildnings-, hjärnskade- och djurstudier i avsikt att ta reda på vilka nervnät och områden i hjärnan som är involverade vid uppkomsten av dystoni [33]. Forskarna konstaterade att olika delar av hjärnan och olika nervnät aktiverades vid olika former av dystoni. De viktigaste delarna av hjärnan är i detta sammanhang basala ganglierna och lillhjärnan.
Finska barnneurologer och neurologer beskrev en 38-årig man, som hade bland annat intellektuell funktionsnedsättning, tremor och dystoni, och som vid en genetisk undersökning (exomsekvensering) visade sig ha en defekt på ARX-genen [34]. Det är känt att denna genetiska defekt orsakar Parlingtons syndrom som är en X-kromosomal sjukdom. Exomsekvensering visade sig vara användbar i detta fall, där man i åratal försökt komma fram till en mer exakt diagnos.
Forskare vid Helsingfors universitet som studerar neurologiska sjukdomar hos barn publicerade en artikel om den roll genetiska eller ärftliga orsaker spelar för progressiva barnneurologiska sjukdomar [35]. De studerade 48 barn hos vilka sjukdomens orsak inte var klarlagd. Patienterna hade många slags progressiva neurologiska symptom; 5 (11 %) hade rörelsestörningar. Studien innebar sekvensering av hela exomet. Hos 20 (42 %) av barnen hittades en avvikande genvariant med koppling till sjukdomen. Åtta av dessa barn visade sig bära på en ny variant. Hos en av patienterna med rörelsestörningar (dyskinesi, myokymi) hittades en avvikande genvariant. Forskarna konstaterade att sekvensering av hela exomet är ett effektivt sätt att hitta orsaken till okända progressiva neurologiska sjukdomar.
Ataxi
I en multinationell studie, med medverkan av forskare från Uleåborg, utreddes olika varianter av en genetisk defekt (ITPR1-genen) som hänger samman med en ärftlig sjukdom i lillhjärnan, spinocerebellär ataxi (SCA) 29, och de sjukdomsformer som orsakas av dessa varianter [36]. Gruppen hittade 46 patienter, bland vilka en del bar på nya varianter. I artikeln beskrivs kliniska fynd och avbildningsfynd hos patienterna.
I en norsk studie, där forskare från Helsingfors universitet medverkade, utreddes effekten av nikotinamid (NAD) ribosid på symptomen vid ataxia telangiectasia hos patienter [37]. Nikotinamid, dvs. niacin eller ett B3-vitamin, behövs bland annat för mitokondriernas funktion. Ataxia telangiectasia är en sällsynt, ärftlig sjukdom som debuterar i barndomen. Sjukdomen förknippas med degeneration av lillhjärnan, immunologiska förändringar samt cancerbenägenhet. Det finns ingen specifik behandling mot denna sjukdom. I studien deltog 13 patienter, av vilka 10 fick nikotinamid ribosid (2×250 mg) i 18 månaders tid. Läkemedlet tolererades väl och ökade NAD-halten i blodet. Under behandlingen konstaterade forskarna en förbättring av motoriken och ögats rörelser. Eftersom studien var öppen och patientantalet litet, är det inte möjligt att dra några långtgående slutsatser om verkan av NAD ribosid. Just nu utförs också studier med denna substans med avseende på Parkinsons sjukdom.
Tremor
Professor Juho Joutsa från Åbo medverkade i en översiktsartikel där man gått igenom fynd från magnetundersökningar som rör essentiell tremor och utgående från dessa dragit slutsatser om nervnät som har samband med tremor [38]. Det framgick att lillhjärnan är den viktigaste knutpunkten för kommunikationsbanorna vid essentiell tremor. Sammanfattningen bekräftar betydelsen av störningar i lillhjärnans funktion för uppkomsten av essentiell tremor.
I sin andra översiktsartikel behandlade professor Juho Joutsa med kollegor betydelsen av lokala skador i hjärnvävnaden och av lesionsbehandlingar vid rörelsestörningssjukdomar [39]. Under årens lopp har kunskapen ökat om vilka slags symptom som följer av skador i ett visst område i hjärnan. Dessutom har man i årtionden använt lesioneringar i talamus (talamotomier) genom upphettning, vid behandling av både essentiell tremor och skakningar vid Parkinsons sjukdom (bild 4).

Bild 4. Tidslinje över lesioner i områden av hjärnan samt lesionering. (Timeline of selected events illustrating the role of lesions in neuroscience and medicine. Top: Spontaneously occurring lesions played a defining role in mapping human brain function, including localization of neurological and psychiatric symptoms. The role of lesions declined with the advent of functional imaging techniques such as PET and functional MRI (fMRI) but is now on the rise due to modern lesion mapping techniques. Bottom: Brain lesions have been used to treat neurological and psychiatric symptoms for nearly one and a half centuries. The therapeutic role of lesions decreased with the development of effective medications and deep brain stimulation (DBS) but is now on the rise due to modern lesioning technologies such as magnetic resonance-guided focused ultrasound (MRgFUS). Note that this timeline is not intended to be comprehensive, but to illustrate the rise, fall and return of lesions. There are exceptions to these historical trends, including DBS treatments explored in 1950s, subthalamic nucleus lesions in 1990, and many lesion studies that occurred during the epoch of functional neuroimaging. DTI=diffusion tensor imaging; PD=Parkinson’s disease.) Ur publikationen Joutsa m.fl. 2023 [39].
Förbättrade avbildningstekniker har ökat kunskapen om samband mellan små hjärnskador och symptom på rörelsestörningar, och man har erhållit information om olika nervnäts betydelse för uppkomsten av sådana symptom. En ny teknik för lesionering är riktad ultraljudsbehandling som inte kräver att skallen öppnas. Skapande av lesioner på ena sidan av talamus med denna teknik är godkänt för behandling av essentiell tremor och skakningar vid Parkinsons sjukdom. I USA är skapande av sådana lesioner på bägge sidor av talamus en godkänd metod för behandling av essentiell tremor. Detta är en bra översiktsartikel som är fritt tillgänglig för alla.
Det är känt att en liten mängd alkohol får händerna att skaka mindre. Alkohol är t.ex. förbjudet inom skytte, eftersom det räknas som dopning. Däremot har man antagit att till och med små mängder alkohol i blodet försämrar förmågan att utföra neurokirurgi. Finska neurokirurger och specialister i neurokirurgi bestämde sig för att bringa klarhet i frågan [40]. De fungerade själva som försökspersoner, intog en liten mängd alkohol och testade sin förmåga att sy igen ett sår, dock inte på patienter utan i ett testlaboratorium. Det framkom att en liten mängd alkohol inte försämrade förmågan att sy; tvärtom blev prestationen den bästa vid en berusning på 0,44 promille! Forskarna insåg att alkoholen minskade de fysiologiska skakningarna, vilket förklarade resultatet. Kanske kan man ändå inte omsätta resultatet i det praktiska arbetet. Detta var en liten studie där de medverkande troligtvis hade roligt!
Huntingtons sjukdom
Docent Jussi Sipilä från Joensuu och professor Kari Majamaa från Uleåborg tog reda på om det under de senaste tio åren skett förändringar i prevalensen av Huntingtons sjukdom i Finland [41]*. Forskningsgruppens tidigare undersökningar har visat att prevalensen av Huntingtons sjukdom är betydligt lägre i Finland än på andra håll i Västeuropa. Man kom i denna studie fram till att prevalensen av Huntingtons sjukdom ligger på 2,57/100 000, en siffra som inte avsevärt skiljer sig från resultatet av föregående studie som slutfördes 2010.
Wilsons sjukdom
Docent Jussi Sipilä undersökte med sina forskningsgrupper genförändringar och symptombilder hos finländare som lider av Wilsons sjukdom [42]. Wilsons sjukdom är en sällsynt, recessivt ärftlig ämnesomsättningssjukdom där koppar ansamlas särskilt i hjärnan, ögonen och levern. Till symptomen hör många slags rörelsestörningar och störd leverfunktion. I studien ingick sex homozygota patienter och elva sammansatt heterozygota patienter. Symptombilden skiljde sig inte åt mellan dessa två grupper, men de homozygota insjuknade i yngre ålder. Allvarlig leverskada hörde samman med en viss genförändring. Den finska patientdokumentationen var en rik källa till information, fastän sjukdomen är mycket sällsynt i Finland.
Docent Fredrik Åberg vid HUS publicerade tillsammans med svenska kollegor en studie om dödlighet vid Wilsons sjukdom [43]. Forskningsunderlag var 151 patienter med Wilsons sjukdom som finns upptagna i register i Sverige. Referensmaterialet utgjordes av 1 441 friska personer. Resultatet var att patienter med Wilsons sjukdom har 3,8 gånger så stor dödlighet jämfört med friska personer. Detta visar att det fortfarande finns stort utrymme för förbättring i behandlingen av Wilsons sjukdom, även om det finns läkemedel som binder koppar.
Tourettes syndrom
Professor Juho Joutsa från Åbo medverkade i en översiktsartikel om de nervnät och anatomiska områden som ligger bakom tics, alltså de tvångsrörelser som förknippas med Tourettes syndrom [44]. Forskningsgruppen samlade ur publikationer platser i hjärnan med skador som är kopplade till tics, och kunde på grundval av dem med sina datorbaserade program kartlägga de viktigaste nervnäten i hjärnan. Det framgick att skadade områden med koppling till tics fanns på flera platser i hjärnan, men att de viktigaste punkterna var i de basala ganglierna. Förbindelserna mellan basala ganglierna, framhjärnan och gördelvindlingen (cingulum) ser ut att fungera onormalt vid Tourettes syndrom. Studien gav många nya insikter i de anatomiska avvikelser som hör samman med Tourettes syndrom. Denna studie är ett tillägg till professor Juho Joutsas högklassiga studier av nervnät (brain mapping).
Experter från Åbo inom talterapi och barnpsykiatri beskrev två pojkar som har en talsvårighet som är kopplad till Tourettes syndrom och påminner om stamning [45]. Experterna lyckades underlätta talet för dessa patienter, med hjälp av talterapi som utvecklats för att behandla stamning.
Neuroepidemiologi
Docent Jussi Sipilä gick i sin publikation igenom neurologiska sjukdomars epidemiologi i Finland utgående från tillgängliga uppgifter [46]. Författaren beskriver hur vissa neurologiska sjukdomar är vanligare i Finland än på andra håll. Till denna grupp hör sjukdomar i det s.k. finländska sjukdomsarvet, men även progressiv myoklonusepilepsi (Unverricht-Lundborgs sjukdom), multipel skleros (MS), amyotrofisk lateralskleros (ALS), spinal muskelatrofi (Jokela-typen) samt dystonier i vuxen ålder. Å andra sidan är vissa sjukdomar mer sällsynta i Finland än annanstans. Detta gäller exempelvis Friedreichs ataxi och Wilsons sjukdom. Tillgängliga uppgifter om många vanliga neurologiska sjukdomar, såsom migrän, Alzheimers sjukdom eller Parkinsons sjukdom, är i någon mån osäkra (bild 5). Avslutningsvis lyfter författaren fram hur bestämmelser i lagen (bland annat lagen om sekundär användning av personuppgifter) och prissättningen på insamling av uppgifter gjort det betydligt svårare att bedriva epidemiologisk forskning i Finland. Artikeln är en bra sammanfattning av finsk neuroepidemiologi.
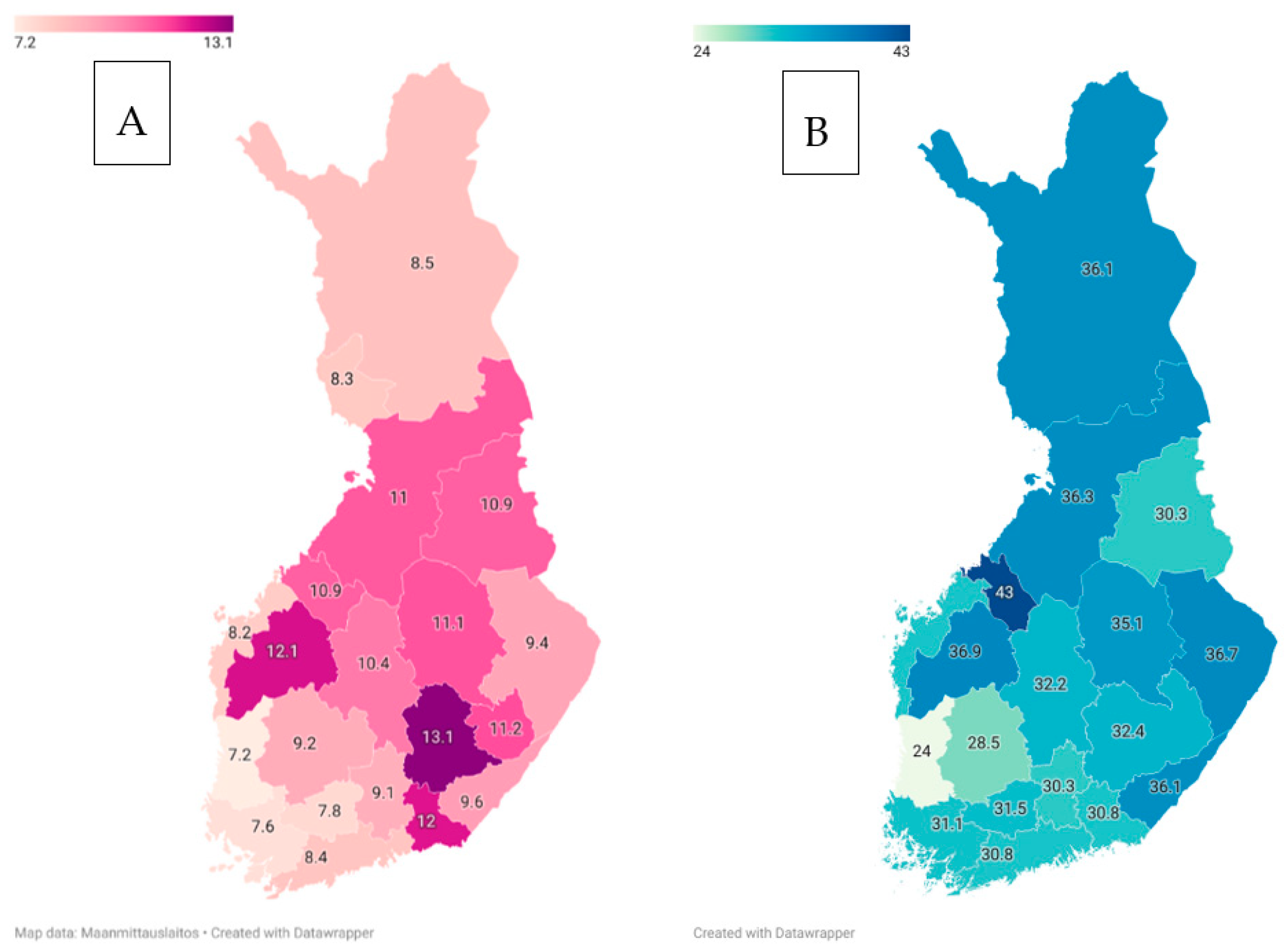
Bild 5. Incidensen av Alzheimers sjukdom (A) och parkinsonism (B) i Finland. ((A) The regional incidence (/100,000) of Alzheimer’s disease in Finland in 2007–2011. (B) The regional incidence (/100,000) of medicated parkinsonism in Finland in 2015–2019). Ur publikationen Sipilä 2023 [46].
Hemifacial spasm
Hemifacial spasm är sammandragningar av musklerna i den ena ansiktshalvan, och beror på störningar i ansiktsnervens funktion. Den vanligaste orsaken är att ett blodkärl tidvis orsakar kompression av ansiktsnerven nära hjärnstammen. Åkomman kan behandlas med botulinumtoxin, eller i vissa fall med blodkärlskirurgi. Hemifacial spasm är till sitt väsen en rörelsestörning, även om åkomman inte räknas som en egentlig rörelsestörningssjukdom.
Neurologer och neurokirurger i Helsingfors har nu klarlagt förekomsten av hemifacial spasm i Finland [47]. De gick igenom patienter som vårdats i HUS område under åren 2014–2019. De hittade 279 patienter, av vilka 62 % var kvinnor och 62 % hade symptom på vänster sida. Hos män var det vanligast att symptomen började uppträda vid en ålder av över 60 år, hos kvinnor vid mer än 80 års ålder. Man kom fram till en årlig incidens på 1,53/100 000 och en årlig prevalens på 10,62/100 000. Detta är en bra finsk studie om ett ämne som det globalt finns begränsad kunskap om.
Studier märkta med asterisk (*) har fått bidrag från Finlands Parkinson-stiftelse.
Författaren är Seppo Kaakkola, prof. (h.c.), neurologin och klinisk farmakologins specialistläkare samt ordförande för Finlands Parkinson-stiftelsens styrelse
Referenser
1. Paakinaho A, Tiihonen M, Koskela H et al. beta2-Adrenoceptor Agonists in Asthma or Chronic Obstructive Pulmonary Disease and Risk of Parkinson’s Disease: Nested Case-Control Study. Clin Epidemiol, 2023. 15: 695-705. https://doi.org/10.2147/CLEP.S405325
2. Pirttila A, Tiihonen M, Paakinaho A et al. Hospitalization and the Risk of Initiation of Antipsychotics in Persons With Parkinson’s Disease. J Am Med Dir Assoc, 2023. 24(9): 1290-1296 e4. https://doi.org/10.1016/j.jamda.2023.04.004
3. Babar BA, Kettunen R, Tiihonen M et al. Prevalence of cardiovascular drugs and oral anticoagulants use among persons with and without Parkinson’s disease. Cardiology, 2023. https://doi.org/10.1159/000535691
4. Ilmaniemi S, Tolppanen AM, Herukka SK et al. Incidence and outcomes of head injuries in people with and without Parkinson disease. Eur J Neurol, 2023. 30(6): 1648-1657. https://doi.org/10.1111/ene.15782
5. Rumrich IK, Lin J, Korhonen A et al. Long-term exposure to low-level particulate air pollution and Parkinson’s disease diagnosis – A Finnish register-based study. Environ Res, 2023. 229: 115944. https://doi.org/10.1016/j.envres.2023.115944
6. Sallmen M, Burstyn I, Uuksulainen S et al. Parkinson’s disease and occupational exposure to organic solvents in Finland: a nationwide case-control study. Scand J Work Environ Health, 2023. https://doi.org/10.5271/sjweh.4125
7. Sipilä JOT, Kaasinen V, Rautava P et al. Case-Fatality Rate in Parkinson’s Disease: A Nationwide Registry Study. Mov Disord Clin Pract, 2023. https://doi.org/10.1002/mdc3.13948
8. Backman EA, Luntamo L, Parkkola R et al. Early cortical atrophy is related to depression in patients with neuropathologically confirmed Parkinson’s disease. J Neurol Sci, 2023. 455: 122804. https://doi.org/10.1016/j.jns.2023.122804
9. Waggan I, Rissanen E, Tuisku J et al. Adenosine A(2A) receptor availability in cerebral gray and white matter of patients with Parkinson’s disease. Parkinsonism Relat Disord, 2023. 113: 105766. https://doi.org/10.1016/j.parkreldis.2023.105766
10. Waggan I, Rissanen E, Tuisku J et al. Adenosine A(2A) receptor availability in patients with early- and moderate-stage Parkinson’s disease. J Neurol, 2023. 270(1): 300-310. https://doi.org/10.1007/s00415-022-11342-1
11. Murtomäki K, Joutsa J, Mertsalmi T et al. Dopamine transporter binding in the brain is linked to irritable bowel syndrome in Parkinson’s disease. Brain Behav, 2023. 13(7): e3097. https://doi.org/10.1002/brb3.3097
12. Ellis EG, Joutsa J, Morrison-Ham J et al. Large-scale activation likelihood estimation meta-analysis of parkinsonian disorders. Brain Commun, 2023. 5(3): fcad172. https://doi.org/10.1093/braincomms/fcad172
13. Suuronen I, Airola A, Pahikkala T et al. Budget-Based Classification of Parkinson’s Disease From Resting State EEG. IEEE J Biomed Health Inform, 2023. 27(8): 3740-3747. https://doi.org/10.1109/JBHI.2023.3235040
14. Huttunen HJ, Booms S, Sjogren M et al. Intraputamenal Cerebral Dopamine Neurotrophic Factor in Parkinson’s Disease: A Randomized, Double-Blind, Multicenter Phase 1 Trial. Mov Disord, 2023. 38(7): 1209-1222. https://doi.org/10.1002/mds.29426
15. Tuunainen J, Sjöstedt N, Vahteristo M et al. Effect of Carbidopa Dose on Levodopa Pharmacokinetics With and Without Catechol-O-Methyltransferase Inhibition in Healthy Subjects. Eur J Drug Metab Pharmacokinet, 2023. 48(1): 23-34. https://doi.org/10.1007/s13318-022-00800-w
16. Viljaharju V, Mertsalmi T, Pauls KAM et al. Levodopa-Entacapone-Carbidopa Intestinal Gel Treatment in Advanced Parkinson’s Disease: A Single-Center Study of 30 Patients. Mov Disord Clin Pract, 2023. https://doi.org/10.1002/mdc3.13926
17. Kähkölä J, Lahtinen M, Keinänen T et al. Stimulation of the Presupplementary Motor Area Cluster of the Subthalamic Nucleus Predicts More Consistent Clinical Outcomes. Neurosurgery, 2023. 92(5): 1058-1065. https://doi.org/10.1227/neu.0000000000002292
18. Kähkölä J, Katisko J, Lahtinen M. Deep Brain Stimulation of Subthalamic Nucleus Improves Quality of Life in General and Mental Health Domains in Parkinson’s Disease to the Level of the General Population. Neuromodulation, 2023. https://doi.org/10.1016/j.neurom.2023.03.007
19. Vollstedt EJ, Madoev H, Aasly A et al. Establishing an online resource to facilitate global collaboration and inclusion of underrepresented populations: Experience from the MJFF Global Genetic Parkinson’s Disease Project. PLoS One, 2023. 18(10): e0292180. https://doi.org/10.1371/journal.pone.0292180
20. Ylikotila P, Sipila J, Alapirtti T et al. Association of biallelic RFC1 expansion with early-onset Parkinson’s disease. Eur J Neurol, 2023. 30(5): 1256-1261. https://doi.org/10.1111/ene.15717
21. Kleine Bardenhorst S, Cereda E, Severgnini M et al. Gut microbiota dysbiosis in Parkinson disease: A systematic review and pooled analysis. Eur J Neurol, 2023. 30(11): 3581-3594. https://doi.org/10.1111/ene.15671
22. Kaasinen V, Luo S, Martinez-Martin P et al. Cross-Cultural Differences in Patient Perceptions of Dyskinesia in Parkinson’s Disease. Mov Disord, 2023. 38(4): 688-692. https://doi.org/10.1002/mds.29335
23. Tavi L, Penttilä N. Functional data analysis of prosodic prominence in Parkinson’s disease: a pilot study. Clin Linguist Phon, 2023: 1-18. https://doi.org/10.1080/02699206.2022.2158372
24. Convey RB, Ihalainen T, Liu Y et al. A comparative study of automatic vowel articulation index and auditory-perceptual assessments of speech intelligibility in Parkinson’s disease. Int J Speech Lang Pathol, 2023: 1-11. https://doi.org/10.1080/17549507.2023.2251725
25. Liikkanen S, Sinkkonen J, Suorsa J et al. Feasibility and patient acceptability of a commercially available wearable and a smart phone application in identification of motor states in parkinson’s disease. PLOS Digit Health, 2023. 2(4): e0000225. https://doi.org/10.1371/journal.pdig.0000225
26. Räty V, Eklund M, Nuuttila S et al. Floating door sign does not differentiate Parkinson’s disease from essential tremor. Clin Park Relat Disord, 2023. 8: 100184. https://doi.org/10.1016/j.prdoa.2023.100184
27. Kuosmanen E, Huusko E, van Berkel N et al. Exploring crowdsourced self-care techniques: A study on Parkinson’s disease. Int J Human-Computer Studies, 2023. 177: 103062. https://doi.org/10.1016/j.ijhcs.2023.103062
28. Ginters M, Talaslahti T, Palm A et al. Criminal Behaviour After Diagnosis of a Neurocognitive Disorder: A Nationwide Finnish Register Study. Am J Geriatr Psychiatry, 2023. 31(8): 598-606. https://doi.org/10.1016/j.jagp.2023.01.025
29. Talaslahti T, Ginters M, Kautiainen H et al. Crime, mortality and neurocognitive disorders: A nationwide register study in Finland. Int J Methods Psychiatr Res, 2023. 32(2): e1948. https://doi.org/10.1002/mpr.1948
30. Kaivola K, Chia R, Ding J et al. Genome-wide structural variant analysis identifies risk loci for non-Alzheimer’s dementias. Cell Genom, 2023. 3(6): 100316. https://doi.org/10.1016/j.xgen.2023.100316
31. Sipilä JOT, Kytövuori L, Rauramaa T et al. A severe neurodegenerative disease with Lewy bodies and a mutation in the glucocerebrosidase gene. NPJ Parkinsons Dis, 2023. 9(1): 53. https://doi.org/10.1038/s41531-023-00501-4
32. Honkanen EA, Ronka J, Pekkonen E et al. GPi-DBS-induced brain metabolic activation in cervical dystonia. J Neurol Neurosurg Psychiatry, 2023. https://doi.org/10.1136/jnnp-2023-331668
33. Corp DT, Morrison-Ham J, Jinnah HA et al. The functional anatomy of dystonia: Recent developments. Int Rev Neurobiol, 2023. 169: 105-136. https://doi.org/10.1016/bs.irn.2023.04.004
34. Arvio M, Lahdetie J, Koivu H et al. Manifestations of Intellectual Disability, Dystonia, and Parkinson’s Disease in an Adult Patient with ARX Gene Mutation c.558_560dup p.(Pro187dup). Case Rep Genet, 2023. 2023: 3636748. https://doi.org/10.1155/2023/3636748
35. Aaltio J, Etula A, Ojanen S et al. Genetic etiology of progressive pediatric neurological disorders. Pediatr Res, 2023. https://doi.org/10.1038/s41390-023-02767-z
36. Tolonen JP, Parolin Schnekenberg R, McGowan S et al. Detailed Analysis of ITPR1 Missense Variants Guides Diagnostics and Therapeutic Design. Mov Disord, 2023. https://doi.org/10.1002/mds.29651
37. Presterud R, Deng WH, Wennerstrom AB et al. Long-Term Nicotinamide Riboside Use Improves Coordination and Eye Movements in Ataxia Telangiectasia. Mov Disord, 2023. https://doi.org/10.1002/mds.29645
38. Younger E, Ellis EG, Parsons N et al. Mapping Essential Tremor to a Common Brain Network Using Functional Connectivity Analysis. Neurology, 2023. 101(15): e1483-e1494. https://doi.org/10.1212/WNL.0000000000207701
39. Joutsa J, Lipsman N, Horn A et al. The return of the lesion for localization and therapy. Brain, 2023. 146(8): 3146-3155. https://doi.org/10.1093/brain/awad123
40. Vasankari V, Eisenring C, Rossmann T et al. Small amount of alcohol did not deteriorate microsurgical dexterity: a prospective laboratory study. Acta Neurochir (Wien), 2023. 165(3): 577-583. https://doi.org/10.1007/s00701-023-05501-0
41. Sipila JOT, Majamaa K. Stable low prevalence of Huntington’s disease in Finland. Clin Park Relat Disord, 2023. 8: 100198. https://doi.org/10.1016/j.prdoa.2023.100198
42. Sipilä JOT, Kytövuori L, Kaasinen V. Clinical spectrum and genotype-phenotype associations in Finnish patients with Wilson’s disease. J Neurol Sci, 2023. 448: 120620. https://doi.org/10.1016/j.jns.2023.120620
43. Aberg F, Shang Y, Strandberg R et al. Four-fold increased mortality rate in patients with Wilson’s disease: A population-based cohort study of 151 patients. United European Gastroenterol J, 2023. 11(9): 852-860. https://doi.org/10.1002/ueg2.12452
44. Zouki JJ, Ellis EG, Morrison-Ham J et al. Mapping a network for tics in Tourette syndrome using causal lesions and structural alterations. Brain Commun, 2023. 5(3): fcad105. https://doi.org/10.1093/braincomms/fcad105
45. Peltokorpi S, Laiho A, Carlson V et al. Effectiveness of speech therapy in treating vocal blocking tics in children with Tourette syndrome: Two case reports. Clin Child Psychol Psychiatry, 2024. 29(1): 301-311. https://doi.org/10.1177/13591045231177433
46. Sipilä JOT. Adult-Onset Neuroepidemiology in Finland: Lessons to Learn and Work to Do. J Clin Med, 2023. 12(12). https://doi.org/10.3390/jcm12123972
47. Nurminen P, Marjamaa J, Niemelä M et al. Incidence and prevalence of Hemifacial Spasm in Finland’s largest hospital district. J Neurol Sci, 2023. 446: 120587. https://doi.org/10.1016/j.jns.2023.120587